Würzburg. Patientinnen und Patienten mit Herzinsuffizienz haben oft mehrere Begleiterkrankungen. Treten mehr als zwei Erkrankungen gleichzeitig auf spricht man von Multimorbidität. Die Häufigkeit von Multimorbidität bei akuter Herzinsuffizienz liegt zwischen 43 % und 98 %, variiert aber je nach geografischer Region. Frühere Berichte über die Auswirkungen von Multimorbidität bei Herzinsuffizienz bezogen sich auf eine begrenzte Anzahl von Ländern, vorwiegend aus Westeuropa, Asien und Nordamerika oder basierten auf Populationen, die an klinischen Studien teilnahmen, bei denen Patientinnen und Patienten mit Komorbiditäten wie schwerer Niereninsuffizienz oder Krebs in der Regel ausgeschlossen waren. In einer im November 2023 im Journal The Lancet Global Health veröffentlichten Analyse unter der Leitung von Prof. Dr. Christiane Angermann vom Deutschen Zentrum für Herzinsuffizienz Würzburg (DZHI) am Uniklinikum Würzburg wurden erstmals weltweit die Häufigkeit von Multimorbidität und ihre Auswirkungen auf die Arzneimitteltherapie und die Prognose untersucht.
82 Prozent der Studienteilnehmenden waren multimorbide
Als Basis für die Analyse diente die Datenbank der prospektiven, multizentrischen Kohortenstudie REPORT-HF (Registry to Assess Medical Practice and Longitudinal Observation for Treatment of Heart Failure). Im Rahmen von REPORT-HF wurden zwischen Juli 2014 und März 2017 in 358 Krankenhäusern aus 44 Ländern auf sechs Kontinenten 18 553 Patienten rekrutiert. Die Dauer der Nachbeobachtung betrug ein Jahr. Dabei benutzen Forschende aus Ägypten, Argentinien, Griechenland, Großbritannien, den Niederlanden, Schweden, Singapur, Norwegen, den USA und Zypern einen einheitlichen Erhebungsbogen. „Fast alle Studienteilnehmende, nämlich 18 528 Patientinnen und Patienten, hatten vollständige Daten zu ihren Komorbiditäten und wurden daher in die Untersuchung einbezogen,“ berichtet Christiane Angermann. „Dabei waren 82 Prozent multimorbide, und wir haben die Länder nach Weltregionen und Einkommensniveaus stratifiziert.“
Mehr Komorbiditäten erschweren die leitliniengerechte Pharmakotherapie
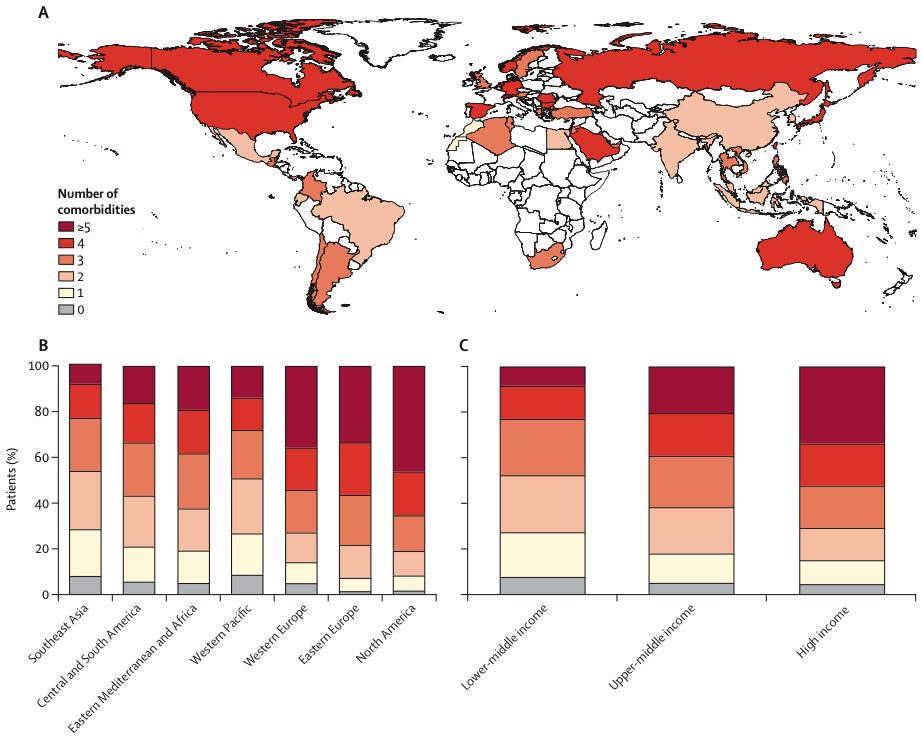
Die Prävalenzraten von Komorbidität waren mit 72 Prozent am niedrigsten in Südostasien und mit 92 Prozent am höchsten in Nordamerika. Patientinnen und Patienten aus Ländern mit niedrigem und mittlerem Einkommen waren seltener multimorbide als Herzinsuffiziente aus Ländern mit hohem Einkommen (73% gegenüber 85%, p<0,0001). Mit zunehmender Multimorbidität erhielten die Betroffenen weniger leitliniengerechte Herzinsuffizienz-Medikamente, dafür aber mehr Medikamente, die eine Herzinsuffizienz verursachen oder verschlechtern können.
Multimorbidität verschlechtert die Prognose
In dieser Studie erwiesen sich Komorbiditäten bei Patientinnen und Patienten, die wegen akuter Herzinsuffizienz in ein Krankenhaus aufgenommen worden waren, als wichtige Prädiktoren, also Vorhersagevariablen, für eine verminderte Lebensqualität, mehr Krankenhausaufenthalte und eine schlechtere Prognose: Die Ein-Jahres-Mortalität stieg von 13 Prozent bei Herzinsuffizienten ohne Komorbiditäten bis auf 26 Prozent, wenn fünf oder mehr Komorbiditäten vorlagen. Der populationsbezogene Anteil der Multimorbidität an der Sterblichkeit, die so genannte ‚population attributable fraction‘, war in Ländern mit hohem Einkommen höher als in Ländern mit mittlerem oder niedrigem Einkommen. Mit 61 Prozent gegenüber 27 Prozent und 31 Prozent hatten hier über die Hälfte aller Todesfälle mit Multimorbidität zu tun.
Ergebnisse unterstreichen systemischen Charakter der Herzinsuffizienz und fordern einen multidisziplinären diagnostischen und therapeutischen Ansatz
Die hohe Prävalenz und enorme prognostische Relevanz der Multimorbidität bei herzinsuffizienten Patientinnen und Patienten aller Weltregionen unterstreichen den systemischen Charakter dieses Syndroms und machen deutlich, dass Komorbiditäten bei der Behandlung der Herzinsuffizienz besondere Aufmerksamkeit verdienen. „Multimorbide Patientinnen und Patienten, die eine Hospitalisierung wegen Herzinsuffizienz überlebt haben, sind nach dieser Analyse weltweit unterversorgt mit den lebensverlängernden Medikamenten, die von den internationalen Leitlinien zur Behandlung der Herzinsuffizienz empfohlen werden. Einerseits wird die Therapie oft unterdosiert, besonders in einkommensschwachen Regionen. Andererseits werden- vor allem in Ländern mit hohem pro-Kopf-Einkommen mit zunehmender Multimorbidität Medikamente gegen diese Krankheiten verschrieben, die ihrerseits Herzinsuffizienz verursachen oder verschlimmern können,“ fasst Christiane Angermann zusammen. „Unsere Ergebnisse machen deutlich, dass Herzinsuffizienz eine lebensgefährliche und komplexe Systemerkrankung ist, deren Behandlung Spezialwissen und einen fachübergreifenden Ansatz erfordert. Multidisziplinäre Betreuungsteams könnten helfen, die medikamentöse Unter- und Fehlversorgung zu vermeiden und die miserable Prognose von Patientinnen und Patienten mit Herzinsuffizienz zu verbessern.“
Publikation
Teresa Gerhardt, Louisa M S Gerhardt, Wouter Ouwerkerk, Gregory A Roth, Kenneth Dickstein, Sean P Collins, John G F Cleland, Ulf Dahlstrom, Wan Ting Tay, Georg Ertl, Mahmoud Hassanein, Sergio V Perrone, Mathieu Ghadanfar, Anja Schweizer, Achim Obergfell, Gerasimos Filippatos, Carolyn S P Lam, Jasper Tromp, Christiane E Angermann, Multimorbidity in patients with acute heart failure across world regions and country income levels (REPORT-HF): a prospective, multicentre, global cohort study, The Lancet Global Health, Volume 11, Issue 12, 2023, Pages e1874-e1884, ISSN 2214-109X, https://doi.org/10.1016/S2214-109X(23)00408-4