Würzburg. Die Erforschung von Blutplättchen (Thrombozyten) und ihrer Vorläuferzellen, den Megakaryozyten, ist ein Paradebeispiel für die Verbindung von Grundlagenwissenschaft und klinischer Medizin. Was vor wenigen Jahrzehnten noch als Randthema galt, ist heute ein zentrales Forschungsfeld mit unmittelbarer gesellschaftlicher Relevanz – und wird sicherlich auch in den kommenden Jahren entscheidend dazu beitragen, Krankheiten besser zu verstehen und wirksamer zu behandeln.
Zahlreiche neue Erkenntnisse und Behandlungsansätze wurden bei der 7th EUPLAN International Conference vorgestellt und diskutiert. Das Treffen des europäischen Blutplättchen-Netzwerks (European Platelet Network) fand vom 17. bis 19. September 2025 im Rudolf-Virchow-Zentrum in Würzburg statt. 150 Wissenschaftlerinnen und Wissenschaftler aus 17 Ländern waren der Einladung von Prof. Dr. Bernhard Nieswandt, Leiter des Instituts für Experimentelle Biomedizin I am Uniklinikum Würzburg (UKW), und Prof. Dr. Markus Bender gefolgt.
Der Lehrstuhl ist auch als „The Würzburg Platelet Group“ bekannt. Insgesamt fünf Arbeitsgruppen beschäftigen sich hier mit der Grundlagen-, translationalen und klinischen Forschung auf dem Gebiet der Thrombozyten- und Megakaryozytenbiologie bei Gesundheit und Krankheit. Ihre Mission ist es, ein umfassendes Verständnis des Thrombozyten-Megakaryozyten-Systems bei thrombotischen, entzündlichen und malignen Erkrankungen zu erlangen, um letztendlich neue Behandlungskonzepte für diese Erkrankungen zu entwickeln.
Hochaktive Akteure in einem komplexen Netzwerk biologischer Prozesse
In einem einzigen Tropfen Blut befinden sich etwa 12 Millionen Thrombozyten. Die kleinen, kernlosen Zellen entstehen im Knochenmark, wo sie von großen, mehrkernigen Zellen, den sogenannten Megakaryozyten, gebildet werden. Ein einzelner Megakaryozyt kann Tausende Thrombozyten produzieren, indem er diese am Ende seiner langen Fortsätze abschnürt. Nach ihrer Freisetzung zirkulieren die Blutplättchen bis zu zehn Tage lang im peripheren Blut, bevor sie abgebaut werden.
In den vergangenen Jahren hat die Forschung immer mehr Funktionen entdeckt, die Blutplättchen in unserem Körper ausüben. Sie sind nicht nur für die lebenswichtige Wundstillung (Hämostase) und die pathologische Gerinnselbildung in unseren Gefäßen (Thrombose) verantwortlich, sondern übernehmen auch zentrale Funktionen bei Entzündungsreaktionen und der Immunabwehr. Die neu gewonnenen Erkenntnisse verändern unser Verständnis von Krankheitsbildern wie Schlaganfällen und Herzinfarkten, aber auch von seltenen Blutungsstörungen, Krebs und Infektionen. Sie tragen dazu bei, neue Therapien zu entwickeln.
Die Würzburg Platelet Group: Bender, Nagy, Nieswandt, Schulze und Stegner
Prof. Dr. Bernhard Nieswandt identifizierte zum Beispiel Thrombozyten als Verursacher für Entzündungsreaktionen im Gehirn nach einem ischämischen Schlaganfall. Er prägte den Begriff der Thrombo-Inflammation, die ein zentraler Pathomechanismus für eine Vielzahl weiterer Erkrankungen ist. Nieswandt und sein Team untersuchen unter anderem, welche Eiweiße auf der Oberfläche der Blutplättchen und welche Signalwege im Zellinneren ihre Aktivität steuern Sie entwickeln neue Therapieansätze, zum Beispiel Antikörper, die gefährliche Blutgerinnsel verhindern sollen.
Prof. Dr. Markus Bender befasst sich unter anderem mit den Mechanismen hinter der sogenannten Thrombozytopenie. Dieser Mangel an Blutplättchen ist ein häufiges klinisches Problem, das mit einem erhöhten Blutungsrisiko verbunden ist. Da Thrombozytentransfusionen lebensbedrohliche Blutungen verhindern können, erforscht Bender mit seinem Team, wie sich eine spenderunabhängige Thrombozytenproduktion optimieren lässt. Weitere Schwerpunkte sind Veränderungen des Zytoskeletts in Thrombozyten, sowohl auf grundlegender als auch auf translationaler Forschungsebene, und wie altersbedingte Entzündungsprozesse im Knochenmark die Funktion von Megakaryozyten und Blutplättchen beeinflussen.
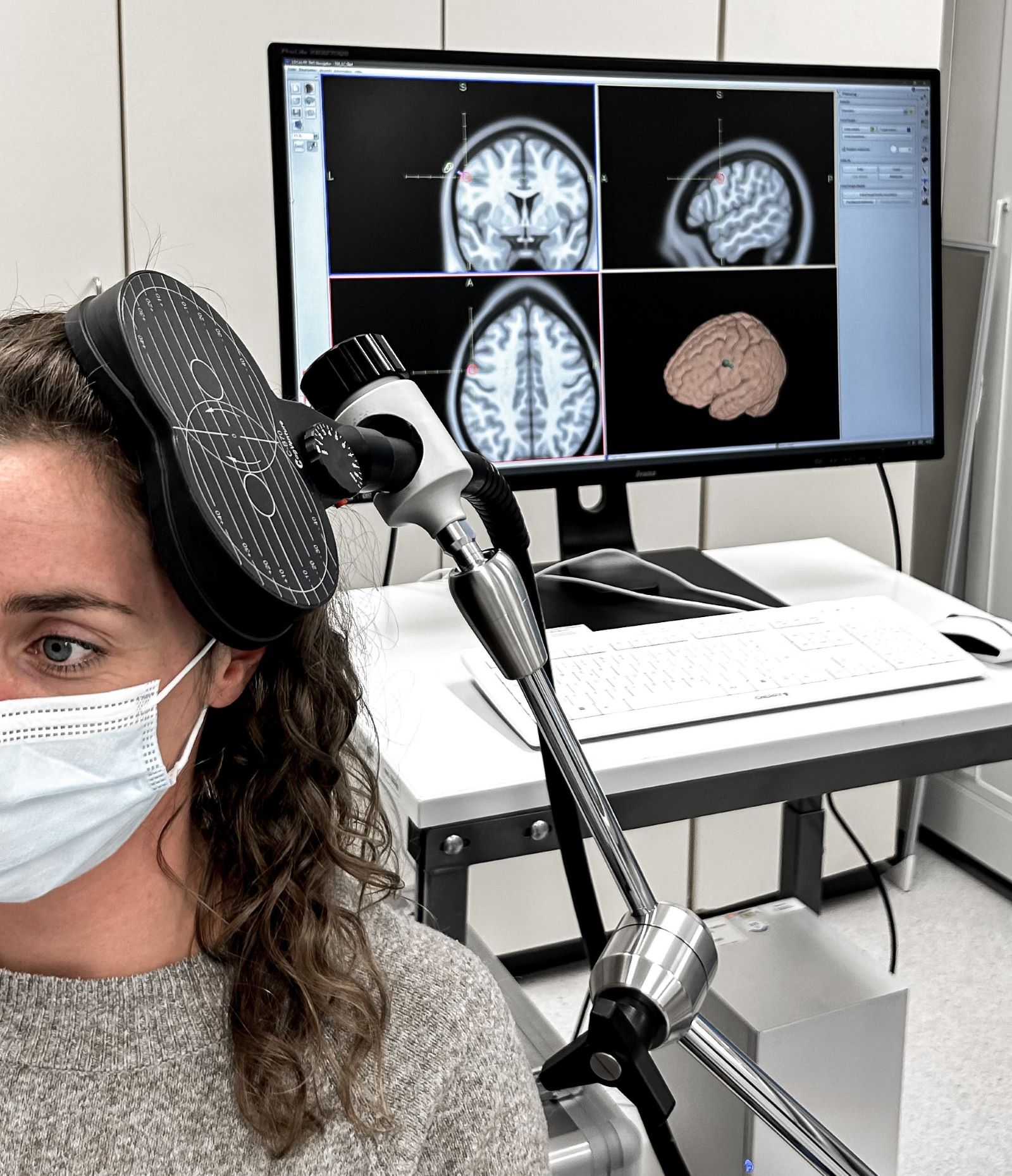
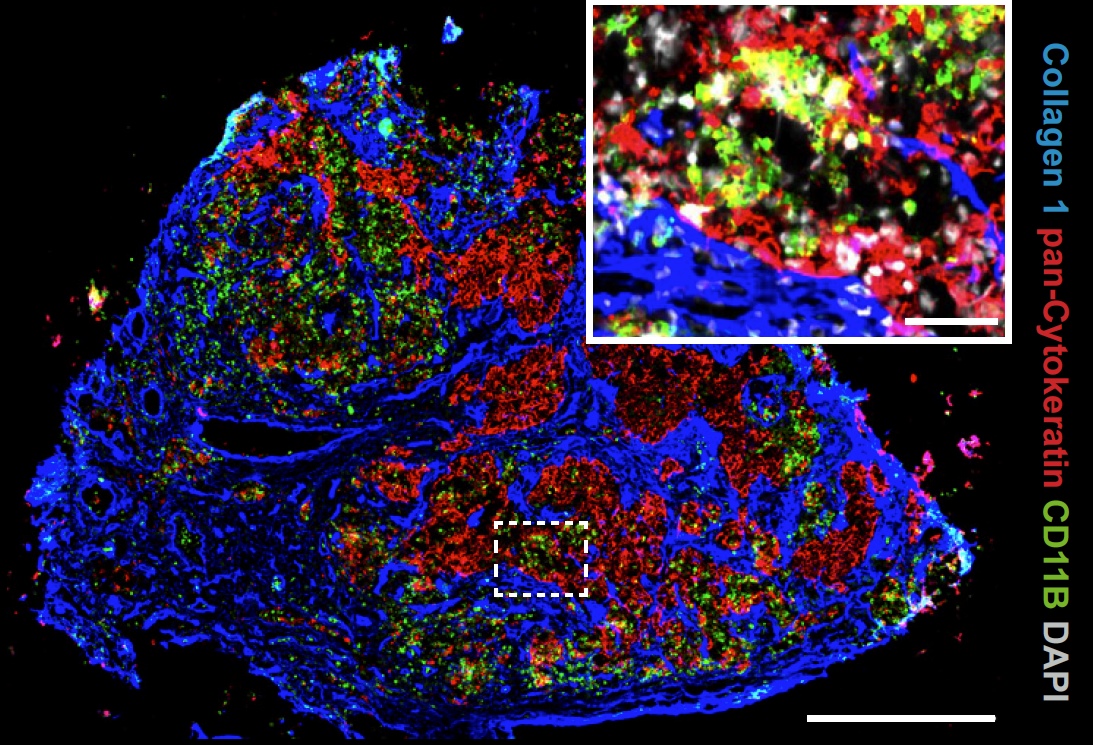
Prof. Dr. David Stegner und seine Arbeitsgruppe machen mithilfe modernster Mikroskopietechniken vaskuläre Prozesse sichtbar und untersuchen, wie Blutplättchen mit Immunzellen zusammenwirken und dabei Entzündungen und Gefäßschäden verursachen, wie sie beispielsweise bei Schlaganfall oder Herzinfarkt auftreten. Das Ziel besteht darin, die zugrundeliegenden Mechanismen besser zu verstehen und neue Behandlungsmöglichkeiten zu entwickeln.
Dr. Zoltan Nagy erforscht mit seiner Emmy-Noether-Forschungsgruppe die Entwicklung und Reifung von Megakaryozyten. Durch ein besseres Verständnis der molekularen Mechanismen der Plättchenbildung möchte er dazu beitragen, Erkrankungen wie Thrombozytopenie oder Knochenmarkfibrose gezielter behandeln zu können. Langfristig streben die Forschenden die Entwicklung neuer Strategien an, um Blutplättchen im Labor herzustellen oder die Plättchenproduktion im Körper zu steigern – ein wichtiger Ansatz angesichts des steigenden Bedarfs an Blutplättchenspenden.
Prof. Dr. Harald Schulze hat seinen Schwerpunkt in der Experimentellen Hämostaseologie, also der Lehre von der Blutgerinnung und ihren Störungen. Mit seiner Arbeitsgruppe erforscht er die Entstehung von Blutplättchen im Knochenmark. Darüber hinaus konzentriert er sich auf Defekte in der Thrombozytenproduktion oder -funktion bei erblichen Blutgerinnungsstörungen beim Menschen sowie bei erworbenen Defekten, wie sie bei Patientinnen und Patienten mit Sepsis oder COVID-19 auftreten. Auf der „7th EUPLAN International Conference“ hielt er eine Keynote-Lecture zum Thema „Thrombozyten-Subpopulationen, Immunthrombose und Thrombo-Inflammation – Wie können wir die Thrombozytenfunktion(en) an der Schnittstelle zwischen Hämostase und Entzündung bestimmen?“
Acht Keynote Lectures auf der 7th EUPLAN International Conference
Insgesamt standen acht Keynote Lectures auf dem Programm. Den Eröffnungsvortrag hielt Prof. Dr. Alessandra Balduini aus Pavia in Italien, die mit ihrem Team ein 3D-Knochenmarkmodell entwickelt hat. Mithilfe dieses Modells ist es möglich, Thrombozyten außerhalb des Körpers zu produzieren und die Mechanismen der Thrombozytenproduktion sowie die Wirkung von Medikamenten zu untersuchen. Für die zweite Eröffnungsrede konnte Prof. Dr. Wolfgang Bergmeier von der US-amerikanischen University of North Carolina gewonnen werden. Er stellte neue Erkenntnisse zur Regulierung der sogenannten Integrinaffinität vor. Dabei handelt es sich um die Bindungsstärke (Affinität) von Zelloberflächenrezeptoren (Integrine).
Aus drei macht eins! Das European Platelet Network EUPLAN
Die EUPLAN International Conference baut auf Konferenzen auf, die bereits in den 1980er Jahren stattgefunden haben. So gab es von 1983 bis 2010 zwölf Konferenzen in Erfurt, die den Titel „Erfurt Conference on Platelets” trugen. Im Jahr 1986 startete zudem in Ascheberg bei Münster eine deutsche Konferenzreihe, die sich später zu einer internationalen Reihe entwickelte und zunehmend auch außerhalb Deutschlands stattfand. Darüber hinaus trafen sich regelmäßig Expertinnen und Experten aus der Thrombozyten-Forschung im Vereinigten Königreich Großbritannien und Nordirland (UK). Im Jahr 2010 wurden in Nottingham (UK) schließlich unter der Federführung von Prof. Stan Heptinstall, einem der führenden Experten auf dem Gebiet der Plättchenphysiologie und -diagnostik, die drei Reihen aus Deutschland und Großbritannien zum großen European Platelet Network (EUPLAN) zusammengeführt, um die grundlegende und klinische Forschung in der Thrombozytenbiologie stärker miteinander zu vernetzen. Die erste EUPLAN-Konferenz fand 2012 in Maastricht (Niederlande) statt. Seither kommen im Zwei-Jahres-Rhythmus Expertinnen und Experten in verschiedenen europäischen Städten zusammen, um sich über ihre wissenschaftlichen Erkenntnisse zu Thrombozyten und ihren Mutterzellen, den Megakaryozyten, auszutauschen.
Damit die dreitägige Konferenz allen offensteht – von etablierten Expertinnen und Experten bis hin zum Forschungsnachwuchs – und der Wissenstransfer nicht an finanziellen Hürden scheitert, sind die Registrierungsgebühren bewusst niedrig gehalten. „Dafür organisieren wir hier alles selbst“, sagt Markus Bender, der den wissenschaftlichen Teil der Konferenz gemeinsam mit Bernhard Nieswandt erarbeitet hat. Für die Administration ist Kerstin Siegmann verantwortlich. Für die Entlastung des Budgets konnten zudem einige Partner aus der Industrie gewonnen werden.
Text: Wissenschaftskommunikation / KL