Würzburg. Das Nierenzellkarzinom ist die häufigste Form von Nierenkrebs bei Erwachsenen. Es entsteht in den Zellen der Nierenkanälchen und kann in fortgeschrittenen Stadien in andere Organe wie Lunge, Leber oder Knochen streuen. Dank moderner Immuntherapien hat sich die Prognose deutlich verbessert – viele Betroffene können heute mehrere Jahre mit der Erkrankung leben. Allerdings spricht jeder fünfte Patient gar nicht auf die Erstlinienbehandlung mit Immun-Checkpoint-Inhibitoren an, und bei weiteren 20 Prozent wird der Krebs innerhalb des ersten Jahres wieder aktiv.
„Die Auswahl der Erstlinientherapie erfolgt gegenwärtig hauptsächlich auf Grundlage einer klinischen Risikoeinschätzung, die Krankheitsverlauf, Laborwerte und Allgemeinzustand berücksichtigt“, erklärt Privatdozent Dr. Charis Kalogirou, geschäftsführender Oberarzt an der Klinik und Poliklinik für Urologie und Kinderurologie des Uniklinikums Würzburg (UKW). „Es gibt jedoch zunehmend Hinweise darauf, dass das Ansprechen auf die Behandlung eher von der Beschaffenheit des Tumors sowie der räumlichen und zellulären Komplexität der Tumormikroumgebung abhängt als vom klinischen Risiko.“
Landkarten des Tumors enthüllen versteckte Immunmuster
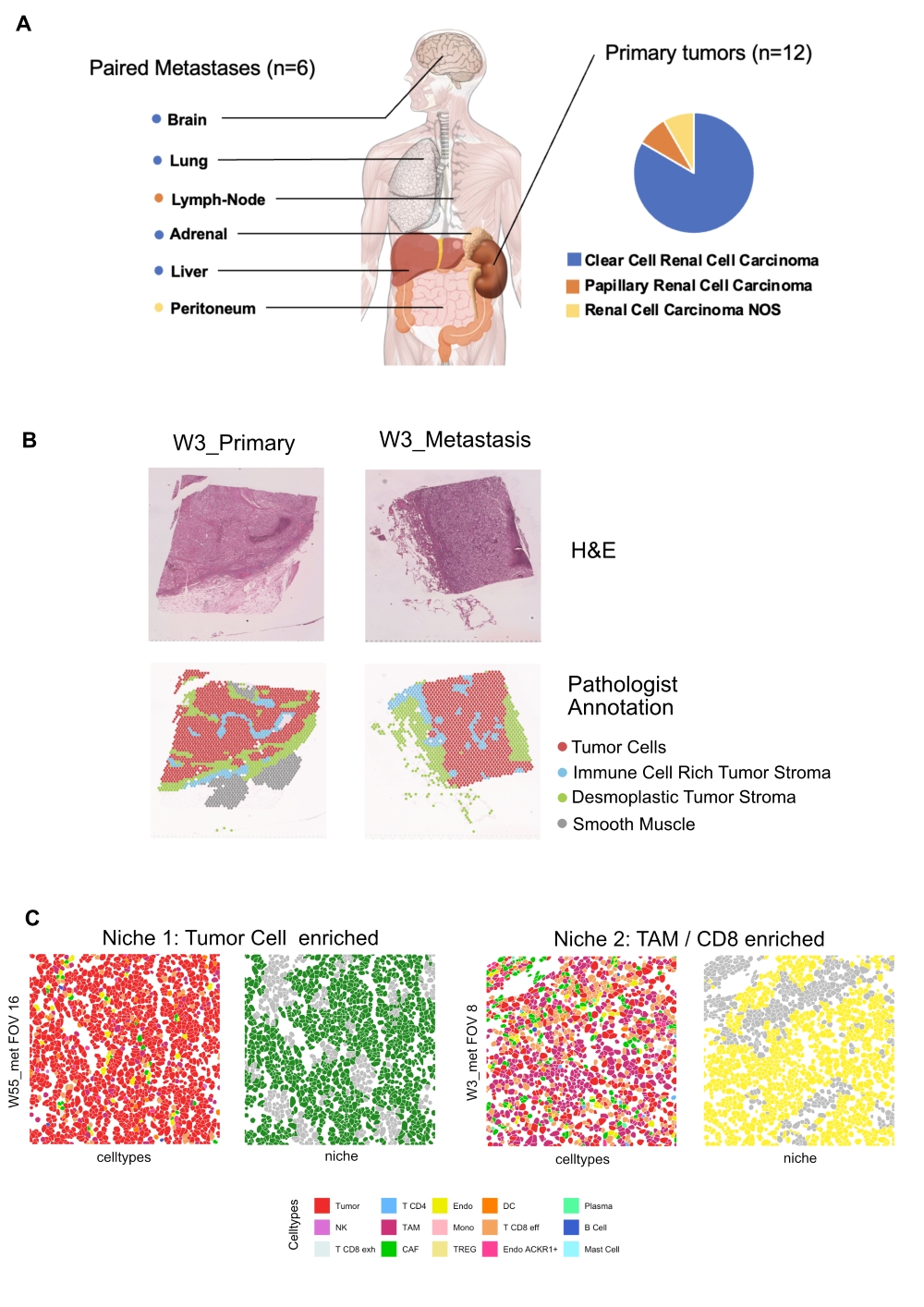
Um diesem Rätsel auf den Grund zu gehen, untersuchten Kalogirou und sein Team Gewebeproben von zwölf Patientinnen und Patienten mit metastasiertem Nierenzellkarzinom, die in der Würzburger Urologie behandelt wurden. Durch den Einsatz hochauflösender räumlicher Transkriptomik gelang es den Forschenden, detaillierte „Landkarten“ des Tumors und seiner Metastasen zu erstellen. Diese zeigen, welche und wie viele Abwehrzellen des Immunsystems sich in der Tumorumgebung befinden, wie aktiv sie sind und wie nah sie an den Krebszellen liegen. Die Ergebnisse veröffentlichten sie jetzt im Journal for ImmunoTherapy of Cancer.
„Wir fanden heraus, dass es nicht nur einen immunen Zustand im Nierentumor gibt, sondern verschiedene lokale Umgebungen mit eigenem Profil“, berichtet Charis Kalogirou, Erstautor der Studie. Selbst Tumoren, die nach herkömmlicher Klassifikation als gleich galten, wiesen erhebliche Unterschiede zwischen einzelnen Patientinnen und Patienten und sogar innerhalb eines Tumors auf. Besonders überraschend: Primärtumor und Metastasen unterschieden sich deutlich in ihrer zellulären Zusammensetzung und räumlichen Anordnung.
„Vor knapp zwei Jahren konnten wir ähnliche Zusammenhänge bereits für das Urothelkarzinom etablieren – und nun auch für das Nierenzellkarzinom“, ergänzt Privatdozent Dr. Markus Eckstein, geschäftsführender Oberarzt am Pathologischen Institut des Uniklinikums Erlangen und Letztautor der Studie. „Insbesondere die Analyse des Immunmikromilieus der Metastasen ist hoch relevant für das Ansprechen auf Immuntherapien und könnte in Zukunft die Therapieselektion deutlich verbessern.“
Günstige Immun-Nischen sagen Therapieerfolg voraus
Die zentrale Entdeckung: In den Metastasen konnten die Forschenden sogenannte „Immun-Nischen“ identifizieren – Bereiche im Tumorgewebe, in denen Makrophagen und CD8+-T-Zellen durch Chemokin-Signale intensiv miteinander interagieren. „Patienten mit diesen Nischen in ihren Metastasen sprachen deutlich besser auf eine Immuntherapie an", erklärt Kalogirou. „In den ursprünglichen Nierentumoren kam diese günstige Nische dagegen kaum vor.“
Eine aus diesen Erkenntnissen abgeleitete Gen-Signatur konnte das Therapieansprechen auch in unabhängigen internationalen Studien mit mehr als 1.000 Patientinnen und Patienten zuverlässig vorhersagen. In Bereichen, die resistent gegen die Therapie blieben, dominierten hingegen Gene, die für eine unterdrückte Immunantwort stehen. Neben der Art der Zellen war auch deren räumliche Anordnung entscheidend – also wie nah die Immunzellen an den Tumorzellen sitzen und welche Gene sie aktivieren.
Präzisere Therapieauswahl in Reichweite
„Es reicht also nicht zu wissen, dass sich Immunzellen im Tumor befinden. Entscheidend ist auch, wo sie sind und wie sie arbeiten“, fasst Charis Kalogirou zusammen. Die Analyse von Metastasen-Biopsien könnte Ärztinnen und Ärzten künftig dabei helfen, besser vorherzusagen, ob ihre Patientinnen und Patienten von einer Immuntherapie profitieren werden. Falls nicht, blieben den Betroffenen weniger wirksame oder nebenwirkungsreiche Behandlungen erspart.
„Dies ist ein wichtiger Schritt hin zu einer präziseren, biomarker-gesteuerten Krebstherapie“, ist Kalogirou überzeugt. Durch die Integration räumlicher Analysen der Tumormikroumgebung in zukünftige Studien könnte die personalisierte Immuntherapie beim metastasierten Nierenzellkarzinom deutlich vorangebracht werden.
Text: Wissenschaftskommunikation / KL