WSelina Vogel und Stella Zankova wurden im Zentrum für Zahn-, Mund- und Kiefergesundheit (ZMK) des Uniklinikums Würzburg zu Zahnmedizinischen Fachangestellten ausgebildet. Aufgrund ihrer guten Kenntnisse und Fähigkeiten konnten beide im Februar 2019 vorzeitig die Abschlussprüfung ablegen. Zudem sprach die Regierung von Unterfranken Selina Vogel für ihren hervorragenden Abschluss der Berufsschule eine besondere Anerkennung aus. Sie kam an der Klara-Oppenheimer-Schule in Würzburg auf eine Abschlussnote von 1,3. Stella Zankova schloss mit einem Notendurchschnitt von 1,7 ab.
„Glücklicherweise konnten wir Selina Vogel für eine Weiterbeschäftigung in der Poliklinik für Zahnärztliche Prothetik gewinnen“, freut sich Prof. Dr. Gabriel Krastl. Der Geschäftsführende Direktor des ZMK gratulierte der frischgebackenen Fachangestellten mit einem Blumenstrauß.
Aktuelle Pressemitteilungen

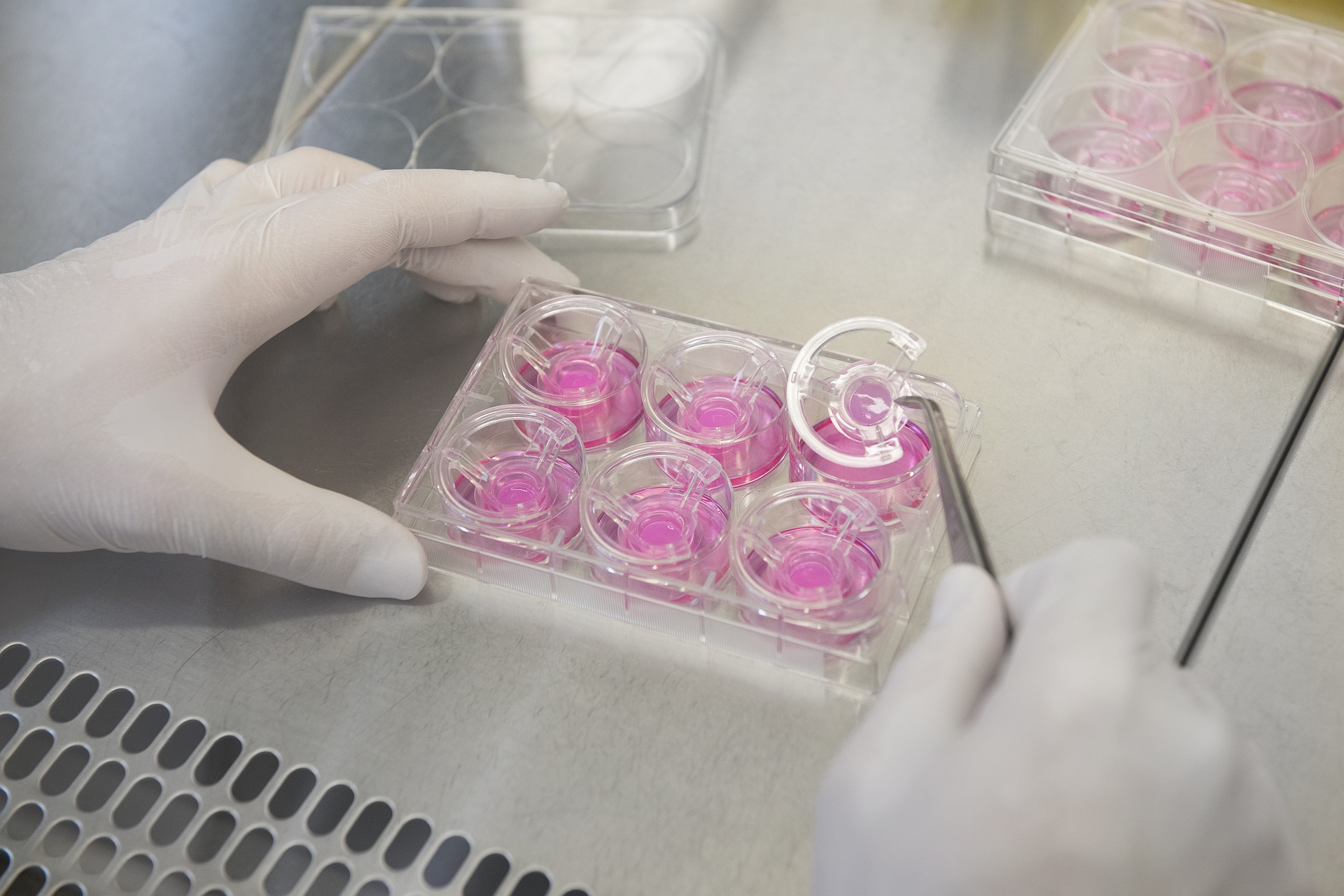
Würzburger Forschungsverbundprojekt will neue Testsysteme für immunonkologische Therapien entwickeln
Innovative immunonkologische Therapien vor dem Einsatz im Mensch noch effizienter in neuen Zellmodellen testen – das ist das Ziel eines Forschungsverbundprojekts. Bei Erfolg könnten durch die Arbeit von Experten des Uniklinikums Würzburg, der Uni Würzburg sowie des Fraunhofer-Instituts für Silicatforschung zudem Tierversuche reduziert werden.
Das Forschungsprojekt ImmuTherM will neue Wege erarbeiten, wie sich die Wirksamkeit von Immuntherapien gegen das Maligne Melanom bestimmen lässt. Hinter dem Vorhaben stehen drei Würzburger Forscher und ihre jeweiligen Teams: Prof. Dr. Bastian Schilling von der Universitäts-Hautklinik, Privatdozent Dr. Niklas Beyersdorf vom Lehrstuhl für Immunologie der Julius-Maximilians-Universität (JMU) sowie Dr. Florian Groeber-Becker vom Fraunhofer-Translationszentrum Regenerative Therapien am Fraunhofer-Institut für Silicatforschung ISC. Das Bundesministerium für Bildung und Forschung (BMBF) fördert das Verbundprojekt im Rahmen des Förderprogramms „Alternativen zum Tierexperiment“ in den kommenden drei Jahren mit insgesamt rund 830.000 Euro.
Immun-Checkpoint-Blocker in der Krebstherapie aussichtsreich
Das maligne Melanom – auch bekannt als „Schwarzer Hautkrebs“ – ist eine der gefährlichsten Krebsarten und führt in Deutschland zu etwa 3.000 Todesfällen pro Jahr. Ein neuer Ansatz zur Behandlung des Melanoms ist die Immuntherapie mit sogenannten Immun-Checkpoint-Blockern (ICB). Immun-Checkpoints sind Rezeptoren auf der Membran von T-Zellen. Sie regulieren die Immunantwort dieser körpereigenen Abwehrzellen, wodurch beispielsweise Autoimmunreaktionen verhindert werden. „Leider sind Tumorzellen in der Lage, diese Checkpoints zu täuschen und dadurch dem Immunsystem zu entkommen“, schildert Bastian Schilling. Der Professor für Dermatologische Onkologie an der Hautklinik des Uniklinikums Würzburg (UKW) fährt fort: „Hier setzen die ICB an, indem sie die Checkpoints blockieren und so die Immunantwort der T-Zellen gegen den Tumor ermöglichen oder verstärken.“
Für die Entdeckung und Nutzbarmachung dieser biologischen Vorgänge für die Krebstherapie ging im Jahr 2018 der Nobelpreis für Medizin an den US-amerikanischen Immunologen James Allison und den japanischen Immunologen Tasuku Honjo. „Das unterstreicht die Bedeutung der Krebsimmuntherapien mit ICB. Umso wichtiger ist es, für den Test der jeweiligen Wirksamkeit dieser Therapien tragfähige Lösungen zu finden“, sagt Prof. Schilling.
Bisherige Testverfahren für die Translation wenig aussagefähig
Bisher konnte der Effekt von ICB in herkömmlichen Zellkultursystemen jedoch noch nicht belegt werden. Das heißt: Gerade für neuartige Immuntherapeutika besteht aktuell eine experimentelle Lücke zwischen der erfolgreichen Etablierung neuer Therapieprinzipien im Tierversuch und der klinischen Erprobung an Probanden oder Patienten, wie Dr. Beyersdorf, Arbeitsgruppenleiter am Institut für Virologie und Immunbiologie der JMU, berichtet.
Ziel: Neue, individuelle Testmodelle aufbauen
Deshalb soll im Forschungsprojekt ImmuTherM ein bereits vom Fraunhofer-Translationszentrum und vom UKW entwickeltes Modellsystem des malignen Melanoms um weitere Tumorzelllinien sowie um humane T-Zellen erweitert werden. „So können im Idealfall individuelle Testmodelle aufgebaut werden, bei denen T-Zellen und Melanomzellen vom selben Patienten stammen“, sagt Dr. Groeber-Becker. Der Leiter des Bereichs In-vitro-Testsysteme am Fraunhofer ISC ergänzt: „Diese neuen individuellen Testmodelle werden anhand von bekannten und bereits als Medikament eingesetzten ICB validiert. Wenn dieser Eignungstest bestanden ist, wird im nächsten Schritt eine neue Immuntherapie, basierend auf einem immobilisierten monoklonalen anti-CD28 Antikörper getestet. So lässt sich überprüfen, ob das Modell geeignet ist, die Wirkung eines noch unbekannten Therapeutikums zu überprüfen.“
Weiterer möglicher Effekt: Tierversuche reduzieren?
Zusammengenommen soll ImmuTherM eine neue Plattform etablieren, um Immuntherapien präklinisch möglichst nahe an der individuellen Patientensituation testen zu können. Sollte eine hohe Vorhersagekraft des Modells belegt werden, so könnte dadurch die Anzahl der benötigten Tierversuche in der frühen präklinischen Phase einer Wirkstoffentwicklung reduziert werden.
Das Vorhaben startet im April dieses Jahres.
Pressekontakt:
Dr. Florian Groeber-Becker, Projektkoordinator, Fraunhofer-Institut für Silicatforschung ISC,
E-Mail: florian.kai.groeber-becker@isc.fraunhofer.de
Marie-Luise Righi, Leitung PR und Kommunikation, Fraunhofer-Institut für Silicatforschung ISC,
E-Mail: righi@isc.fraunhofer.de
Dr. Esther Knemeyer Pereira, Leiterin der Pressestelle der Julius-Maximilians-Universität Würzburg,
E-Mail: esther.knemeyer@uni-wuerzburg.de



Das Spektrum an möglichen Nebenwirkungen der Krebstherapie ist breit. Der Ausfall und die Strukturveränderung der Haare unter Chemotherapie sind da fast schon „Klassiker“. Hinzukommen können allerdings auch Ausschläge, Entzündungen und Pigmentveränderungen an der Haut. „Diese Probleme können insbesondere bei neuen Behandlungsmethoden, wie der Immuntherapie und anderen personalisierten Therapien, auftreten“, weiß Dr. Anja Gesierich. Die Oberärztin am Hautkrebszentrum des Uniklinikums Würzburg fährt fort: „Durch ein gutes Nebenwirkungsmanagement ist es möglich, einen großen Teil dieser Belastungen abzumildern. Dies ist ein wichtiger Beitrag dazu, dass die Patienten ihre Therapien auch im erforderlichen Umfang erhalten können.“
Die Ursachen den jeweiligen Nebenwirkungen an Haut und Nägeln sowie ihre Vermeidungsstrategien erläutert Dr. Gesierich bei einer kostenlosen Patientenveranstaltung des am Uniklinikum Würzburg angesiedelten Comprehensive Cancer Centers Mainfranken am Mittwoch, den 10. April 2019, zwischen 17:00 und 18:00 Uhr. Neben einem Vortrag gibt es ausreichend Gelegenheit für Tumorpatienten, ihre Angehörigen sowie sonstig Interessierte, Antworten auf individuelle Fragen zu bekommen.
Veranstaltungsort ist die Würzburger Universitäts-Hautklinik, Haus D8 an der Josef-Schneider-Straße. Anmelden kann man sich unter Telefon: 0931/20135350 oder E-Mail: anmeldung_ccc@ukw.de.



Herz-Kreislaufkrankheiten treten mit zunehmendem Alter immer häufiger auf. Aber nicht nur Herz und Blutgefäße altern, sondern auch das Immunsystem, man spricht dann von einer Immunoseneszenz. „In den bisherigen experimentellen Studien wurde vornehmlich junges und gesundes Biomaterial untersucht, was nicht unbedingt die klinische Situation widerspiegelt“, erläutert Dr. Gustavo Ramos, Biologe am Deutschen Zentrum für Herzinsuffizienz Würzburg (DZHI) am Uniklinikum Würzburg (UKW). In seinem neuen von der DFG geförderten Forschungsprojekt möchte er daher die Rolle von speziellen Immunzellen, den T-Zellen, nach einem Myokardinfarkt im alten Organismus untersuchen. „Wir konnten in den vergangenen Jahren zeigen, dass die T-Zellen als Helferzellen des Immunsystems eine frühe Heilung nach einem Herzinfarkt in jungen Versuchstieren unterstützt“, erklärt Ramos. „Andererseits fördern diese T-Zellen aber auch altersbezogene Umbauvorgänge im Herzen. In unserem DFG-Projekt möchten wir deshalb die Bedeutung der Immunoseneszenz für die Infarktheilung untersuchen.“
Der 37-Jährige hat in Brasilien Biologie studiert und im Fach Pharmakologie promoviert. Immunologische Aspekte standen schon früh im Fokus seiner Forschung. Von der Immunologie in der Evolution im Allgemeinen kam er schließlich zum Herzen im Speziellen und im Jahr 2013 nach Würzburg. Am Uniklinikum Würzburg wird bereits seit mehr als 30 Jahren an entzündlichen Prozessen im Herzen geforscht, und es findet seit langem eine enge Zusammenarbeit der Fachbereiche Immunbiologie und Kardiologie statt.
Einer, der seit den 1990er Jahren an diesem Thema arbeitet und die Arbeit von Gustavo Ramos unterstützt, ist Professor Stefan Frantz, Leiter der Medizinischen Klinik und Poliklinik I am Uniklinikum Würzburg: „Wir wissen seit langem, dass Patienten nach einem Herzinfarkt unterschiedlich gute Heilungsverläufe aufweisen. Nun gilt es herauszufinden, welche Faktoren die Heilungsprozesse wie fördern oder behindern, und wie man diese rechtzeitig erkennen und die Heilung positiv beeinflussen kann.“
Die Förderung des neuen ERA-Forschungsprojekts kommt da gerade recht: „Ich freue mich sehr, dass wir gemeinsam mit Professor Peter Rainer von der Medizinischen Universität Graz und Professor Encarnita Mariotti-Ferrandiz von der Sorbonne Université Paris nach neuen immunbasierten Prognosewerkzeugen und innovativen Behandlungskonzepten für Herzinfarkt-Patienten suchen können“, kommentiert Gustavo Ramos den Beginn des interdisziplinären Forschungsprojekts und erläutert das Dreigestirn: „In Graz befindet sich neben einer ausgezeichneten Kardiologie mit dem Diagnostik- und Forschungsinstitut für Pathologie eine umfangreiche Biobank. In Paris ist der immunologische Schwerpunkt, hier wurde einst der AIDS-Virus entdeckt. Würzburg fungiert als Schnittstelle von Immunologie und Kardiologie.“
Gemeinsam werden die Wissenschaftler die T-Zellen und ihr ambivalentes Verhalten unter die Lupe nehmen. Dazu sollen mithilfe des genanalytischen Verfahrens Next-Generation-Sequencing spezifische T-Zell-Profile identifiziert werden, die einen prognostischen Nutzen bringen und helfen, die guten von den schlechten „Heilern“ zu unterscheiden. Ziel ist es, einen Biomarker zu entwickeln, mit dem sich die Qualität des Heilungsprozesses erkennen lässt und eine T-Zell-basierte Therapie zu finden, mit der die kardiale Heilung verbessert werden kann.
Pressemitteilung als PDF.
Hier bekommen Sie weitere Informationen zur Juniorforschungsgruppe von Gustavo Ramos.

Das Projekt „PAIN 2020“ der Deutschen Schmerzgesellschaft e. V. und der Krankenkasse Barmer wird vom Innovationsfond des Gemeinsamen Bundesausschusses (GBA) gefördert. Es zielt darauf ab, die Versorgungsqualität und Versorgungseffizienz für Patienten mit Risikofaktoren für chronifizierende Schmerzen zu verbessern. Das an der Klinik und Poliklinik für Anästhesiologie des Uniklinikums Würzburg (UKW) angesiedelte Zentrum für interdisziplinäre Schmerzmedizin (ZIS) beteiligt sich an dieser Studie und sucht derzeit weitere Teilnehmer/innen. Zielgruppe sind Patienten mit Schmerzen, die ein erhöhtes Risiko für eine Chronifizierung aufweisen. Für eine Aufnahme in die Studie gelten folgende Bedingungen:
• Die potenziellen Teilnehmer/innen müssen mindestens 18 Jahre alt sein.
• Sie leiden seit mehr als sechs Wochen unter Schmerzen oder Schmerz-Rezidiven trotz fachspezifischer Behandlung.
• Der Schmerz schränkt ihre Lebensabläufe und ihre Lebensqualität ein.
• Sie sind entweder aktuell seit vier Wochen arbeitsunfähig oder haben eine kumulierte Arbeitsunfähigkeit von mindestens sechs Wochen in den vergangenen zwölf Monaten.
• Sie sind bei der Barmer Ersatzkasse versichert.
Multiprofessionelles Assessment als Kernelement
Bei der Studie erwartet sie ein multiprofessionelles Assessment – eine ärztliche, physiotherapeutische und psychologische Einschätzung der Beschwerden – unter einem Dach. Das Assessment am ZIS dauert etwa einen halben Tag. Die Experten besprechen das Ergebnis der Einschätzung mit dem Patienten. Anschließend wird gemeinsam entschieden, wie es weitergeht. Unter Umständen kommt eines der beiden neuen, im Rahmen von PAIN 2020 angebotenen ambulanten Therapiemodule in Frage. Option eins ist eine einmalige, dreistündige Schulung, Option zwei ein zehnwöchiges Gruppenprogramm. Die Sitzungen finden jeweils am frühen Abend statt und lassen sich also gut mit einer Berufstätigkeit vereinbaren. Bei beiden Therapieoptionen arbeiten Ärztinnen und Ärzte, Physiotherapeut/innen sowie Psycholog/innen eng zusammen. Ziel ist es, den Patienten selbst zum Experten für seine Beschwerden und den Umgang damit zu machen.
Die Teilnahme an der Versorgungsstudie „PAIN 2020“ ist kostenlos. Für weitere Informationen kontaktieren Interessierte das Zentrum für Interdisziplinäre Schmerzmedizin des Uniklinikums Würzburg unter Telefon: 0931 / 201-30300 oder E-Mail: PAIN2020@ukw.de. Zusätzliche Details finden sich unter www.pain2020.de
Das von der Deutschen Krebshilfe zertifizierte Prostatakarzinomzentrum des Uniklinikums Würzburg (UKW) lädt am Samstag, den 6. April 2019, wieder alle Interessierten dazu ein, wissenswerte Hintergründe und neue Erkenntnisse über die häufigste Krebsart des Mannes zu erfahren. Zwischen 10:00 und 14:00 Uhr werden neun Experten im Hörsaal des Zentrums für Operative Medizin (ZOM) an der Oberdürrbacher Straße zu diversen Aspekten referieren und die Fragen der Zuhörer/innen beantworten.
Diagnostik mit PSA und PSMA
Beispielsweise wird Dr. Arkadius Kocot über die Bedeutung des PSA-Wertes in der Prostatakrebsvorsorge informieren. „Auch wenn die routinemäßige PSA-Wertbestimmung wegen relativ häufiger falsch positiver Befunde nach wie vor umstritten ist, gibt es Studien, die belegen, dass über die Messung des Prostataspezifischen Antigens die Sterblichkeit am Prostatakarzinom reduziert werden kann“, schildert der Leitende Oberarzt der Urologischen Klinik des UKW.
Das Prostata-spezifische Membran Antigen (PSMA) gilt als ideales Zielmolekül für die Diagnostik sowie für zielgerichtete Therapien von Prostatakrebs. Prof. Dr. Andreas Buck, der Direktor der Klinik und Poliklinik für Nuklearmedizin des UKW, wird beim Infotag die Untersuchungsmöglichkeiten verdeutlichen, die sich aus der Kombination von PSMA und PET-CT ergeben.
Multiparametrisches MRT und Fusionsbiopsie
Eine weitere, vor allem in der Primärdiagnostik aussagefähige Untersuchungsmöglichkeit ist die multiparametrische Magnetresonanztomographie (mpMRT). Dr. Florian Schneider, Oberarzt der Klinik für Radiologie am UKW, wird die Vorteile dieser Technik darstellen.
Durch die hochauflösende mpMRT ist es möglich, bösartige Veränderungen in der Prostata mit hoher Genauigkeit zu identifizieren. Anschließend können diese Veränderungen mithilfe einer Probenentnahme aus der Prostata – einer Biopsie – weiter abgeklärt werden. Privatdozent Dr. Georgios Hatzichristodoulou, Oberarzt der Klinik und Poliklinik für Urologie und Kinderurologie des UKW, wird über die Technik und die Vorteile der modernen Fusionsbiospie berichten.
Aktuelle Therapieoptionen
Medikamentös, radiologisch, operativ – für Prostatakrebs steht eine vergleichsweise breite Palette an Therapieoptionen zur Verfügung. Am Infotag erläutert die UKW-Urologin Dr. Anna Seitz die medikamentösen Behandlungschancen des metastasierten Prostatakarzinoms. Den „State of the Art“ bei operativen Verfahren schildert Prof. Dr. Hubert Kübler, der Direktor der Urologischen Universitätsklinik, während Dr. Bülent Polat, Oberarzt der Klinik und Poliklinik für Strahlentherapie, die Chancen und Vorteile der primären Strahlentherapie beschreibt.
Selbsthilfe und Psychoonkologie
Darüber hinaus werden am 6. April auch komplementäre Gesichtspunkte angesprochen, wie zum Beispiel die Leistungen der Selbsthilfegruppe Prostatakrebs Würzburg. Außerdem wird die Psychoonkologin Dr. Elisabeth Jentschke aufzeigen, welche psychischen Hilfen es für Prostatakrebs-Patienten gibt.
Die Teilnahme am Patienteninfotag ist kostenlos, das detaillierte Programm gibt es unter www.urologie.ukw.de, Rubrik „Veranstaltungen“.


T-Zellen sind weiße Blutkörperchen, die der Immunabwehr dienen. Leider sind sie in ihrem natürlichen Zustand für Tumorzellen „blind“. Durch gentechnologische Veränderungen können sie allerdings für jeweils eine spezifische Krebsart maßgeschneidert „scharfgestellt“ werden (siehe Kasten). Diese CAR-T-Zellen sind in den letzten Jahren in den Fokus der internationalen Krebstherapieforschung und der biopharmazeutischen Entwicklung gerückt. Das Uniklinikum Würzburg (UKW) arbeitet hier seit einigen Jahren in der Weltelite mit – sowohl in der präklinischen Entwicklung, wie auch in der Anwendung der ersten einsatzfähigen Präparate.
„In diesem Zusammenhang war es eine überaus weitsichtige Entscheidung von Prof. Dr. Hermann Einsele – dem Direktor der Medizinischen Klinik II und selbst ein Pionier der zellulären Immuntherapie – im Jahr 2012 Dr. Michael Hudecek aus den USA an unser Klinikum zu holen“, unterstreicht Prof. Dr. Georg Ertl. Der Ärztliche Direktor des UKW präzisiert: „Auf der Basis von Dr. Hudecek‘s Know-how in der CAR-T-Zell-Forschung konnten ein Forschungslabor und eine Arbeitsgruppe zu diesem neuartigen Arzneimittelprinzip aufgebaut werden, die sich heute großer internationaler Sichtbarkeit erfreuen.“ Prof. Dr. Matthias Frosch, der Dekan der Medizinischen Fakultät zeigt sich begeistert von den Publikationen der Arbeitsgruppe in hochrangigen Fachjournalen und der erfolgreichen Drittmitteleinwerbung in diesem Bereich.
Teil der Forschungs-Weltelite
Gemessen werden kann diese „Sichtbarkeit“ zum Beispiel daran, dass Prof. Einsele und Dr. Hudecek regelmäßig zu Kongressen in aller Welt eingeladen werden, um vor der immunonkologischen Weltelite ihre Ergebnisse zu präsentieren. Zuletzt organisierten die beiden Experten im Februar dieses Jahres das erste europäische CAR-T-Zell-Meeting in Paris/Frankreich, wo sie selbst mehrere Vorträge hielten.
Ein weiteres „Qualitätsmerkmal“ der Würzburger CAR-T-Zell-Forschung ist die erfolgreiche Einwerbung von Forschungs-Drittmitteln aus unterschiedlichen Quellen – sowohl von der Deutschen Krebshilfe und dem Bundesministerium für Bildung und Forschung, wie auch von der Europäischen Union.
Mit etwa 20 Mitarbeiterinnen und Mitarbeitern – Wissenschaftlern, Medizinern, Medizinisch-technischen Angestellten, Doktoranden sowie Gastwissenschaftlern aus anderen europäischen Ländern – ist die Arbeitsgruppe von Dr. Hudecek eines der größten präklinischen Programme zu CAR-T-Zellen in Europa.
An großen internationalen Studien beteiligt
Auch die Translation, also der Einsatz neuer Präparate im Patienten, gelingt in Würzburg. So ist das UKW an einer internationalen und multizentrischen Phase I/IIa klinischen Studie beteiligt. Hauptziel des EURE-CART-Projekts ist der Nachweis der Sicherheit und Effektivität eines CAR-T-Zell-Produktes zur Behandlung der Akuten Myeloischen Leukämie und des Multiplen Myeloms.
Parallel dazu leitet die Medizinische Klinik II des Uniklinikums Würzburg das von der EU geförderte Projekt CARAMBA. Das ebenfalls multinational aufgestellte Projekt zielt darauf ab, ein von Dr. Hudecek entwickeltes CAR-T-Zellen-Produkt für die Behandlung des Multiplen Myeloms in die klinische Anwendung zu überführen.
Anwender zugelassener Bio-Pharma-Präparate
Mittlerweile haben mehrere (Bio-)Pharmaunternehmen für eine Reihe von CAR-T-Zell-Präparaten die Zulassung in den USA und Europa erhalten. Das UKW gehört hier zu den wichtigsten Anwendern in Deutschland. „Seit dem Jahr 2016 behandeln wir als eine der ersten deutschen Einrichtungen Patienten mit zugelassenen CAR-T-Zell-Produkten. Bislang haben wir insgesamt 20 Menschen mit Lymphknotenkrebs oder akuter lymphatischer Leukämie therapiert, bei denen alle etablierten Therapien versagt hatten“, berichtet Prof. Einsele.
Erfolgsbeispiel eines Myelom-Patienten
Im letzten Jahr wurden am UKW zudem die ersten beiden Myelom-Patienten mit von der Industrie bereitgestellten CAR-T-Zellen behandelt. Einer davon ist Peter J. aus dem Raum Schweinfurt. Bei dem heute 70-Jährigen wurde die bösartige Krebserkrankung des Knochenmarks Ende des Jahres 2015 diagnostiziert. Ab Mai 2016 erhielt er an der Medizinischen Klinik II des UKW mehrere Chemotherapien und wurde in Abständen drei Mal mit Eigenstammzellen therapiert. „Leider kehrten die Myelom-Zellen danach immer schneller zurück. Die Behandlung mit CAR-T-Zellen war für Herrn J. eine der letzten verbleibenden Behandlungsoptionen“, schildert Prof. Einsele und fährt fort: „Glücklicherweise passte er in eine entsprechende Studie eines US-amerikanischen Biopharmazie-Unternehmens.“ Anfang Dezember 2018 wurden ihm seine in den USA entsprechend modifizierten und vermehrten T-Zellen zurückinfundiert. Außer einer zeitweiligen Fieberreaktion kam es zu keinen Nebenwirkungen. Hingegen sank die Menge der Myelom-Zellen in seinem Körper drastisch ab. Seit Mitte Januar 2019 ist Peter J. wieder zu Hause und fühlt sich den Umständen entsprechend sehr gut. Er ist schmerzfrei und kann bis zu einer Stunde problemlos spazieren gehen sowie leichte körperliche Arbeiten verrichten. Für eine weitere „Normalisierung“ muss in den kommenden Wochen und Monaten noch sein therapiebedingt zurückgedrängtes Immunsystem wieder aufgebaut werden.
Wie bei Peter J. sind die Ergebnisse der CAR-T-Zell-Therapien am UKW insgesamt sehr positiv. „Bei einem Großteil unserer Patienten konnten wir eine Remission erreichen. Das bedeutet, dass die Tumoren nach einer einmaligen CAR-T-Zell-Gabe so weit zurückgehen, dass man dauerhaft keine Krebszellen mehr nachweisen kann“, erläutert Dr. Hudecek.
Entwicklungsziele: Feinschliff und Ausweitung
Zu den Forschungszielen der nächsten Zeit zählt es, die bestehenden CAR-T-Zell-Produkte noch weiter zu verfeinern und noch besser steuerbar zu machen. „Hier kommen die Synergien zwischen unserer präklinischen und klinischen Arbeit sowie die gute Kooperation mit der Industrie zum Tragen. Beispielsweise arbeiten wir in unserem Labor daran, das Nebenwirkungsmanagement von vorhandenen CAR-T-Zell-Präparaten weiter zu optimieren“, sagt Prof. Einsele.
Eine weitere Hauptaufgabe sieht der Klinikdirektor ferner darin, das Anwendungsspektrum von CAR-T-Zellen zukünftig auf möglichst jede Krebsart auszuweiten. So untersucht die Medizinische Klinik II des UKW derzeit, ob dieses Arzneimittelprinzip auch bei soliden Tumoren wie Brust-, Lungen- oder Bauspeicheldrüsenkrebs hilfreich sein kann.
Durch regionale Spenden- und Stiftungsgelder gefördert
Eine besondere „Rückenstärkung“ für die Würzburger CAR-T-Zell-Forschung war und ist die Förderung durch den Verein ‚Hilfe im Kampf gegen Krebs‘ und die Stiftung „Forschung hilft“. So organisierte der von Gabriele Nelkenstock geführte Verein bereits im Jahr 2013 auf der Mainfranken-Messe in Würzburg einen Benefizlauf, dessen Erlös gezielt dem Projekt von Dr. Hudecek zugute kam. „Schon damals zeichnete sich ab, welche große Bedeutung CAR-T-Zellen für zukünftige Krebstherapien haben können. Deshalb war es Hilfe im Kampf gegen Krebs e.V. ein Anliegen, die Weiterentwicklung des Projektes im Rahmen unserer Möglichkeiten zu sichern und voranzutreiben“, berichtet Gabriele Nelkenstock.
Fortgesetzt wurde die Förderung durch die im Jahr 2017 gegründete Stiftung „Forschung hilft“. Hinter der Einrichtung stehen der Verein „Hilfe im Kampf gegen Krebs“ und die Medizinische Fakultät der Julius-Maximilians-Universität Würzburg (JMU). Im vergangenen Jahr ehrte die Stiftung insgesamt sieben wissenschaftliche Arbeitsgruppen mit Förderpreisen. Sehr großen Zuspruch fand beim externen wissenschaftlichen Beirat der Stiftung das Designer-T-Zellen-Projekt von Dr. Hudecek. Entsprechend erhielt es eine Fördersumme von 20.000 Euro. „Diese Unterstützung ist für uns in mehrfacher Hinsicht wertvoll“, so Dr. Hudecek. Zum einen seien die Gelder höchst willkommen, um neue Ideen seiner Arbeitsgruppe zügig testen zu können – ohne langwierige Förderungsanträge. „Zum anderen sehen wir die Förderung auch als eine besondere, von der regionalen Bevölkerung getragene Wertschätzung unserer Arbeit, die uns zusätzlich motiviert“, beschreibt der Forscher. „Die Universität Würzburg ist dem Verein ‚Hilfe im Kampf gegen den Krebs‘ überaus dankbar für die Einrichtung der Stiftung zur Förderung der Krebsforschung. Damit können zukunftsweisende, erfolgversprechende Ansätze in der Krebsforschung der JMU vertieft und ausgebaut werden“, betont Prof. Dr. Alfred Forchel, Präsident der Universität Würzburg.
So funktioniert die CAR-T-Zell-Therapie
Für die Herstellung von CAR-T-Zellen werden zunächst T-Zellen aus dem Blut des Patienten gewonnen. Mit gentechnischen Verfahren wird in die Zellen ein neues Gen stabil eingebaut, das T-Zellen normalerweise nicht haben. Dieses Gen ist der Bauplan für ein spezifisches Protein, das als künstlicher (chimärer) Antigenrezeptor (CAR) bezeichnet wird. Die modifizierten T-Zellen werden zur Vermehrung angeregt und dem Patienten über eine Infusion wieder zugeführt. Mithilfe des künstlichen Antigenrezeptors erkennen die CAR-T-Zellen gezielt die Tumorzellen, docken an diesen an und töten sie ab. Vor der Rückgabe der CAR-T-Zellen wird in der Regel eine intensive Chemotherapie durchgeführt. Sie drängt nicht nur die Tumorzellen zurück, sondern auch das körpereigene Immunsystem. So können sich die CAR-T-Zellen effektiver im Körper des Patienten vermehren.



