Viele Menschen mit Schizophrenie haben jedoch Schwierigkeiten, solche Bewegungen korrekt auszuführen oder zu verstehen. Dies kann ihre sozialen Kontakte und Alltagsfähigkeit beeinträchtigen. Prof. Dr. Sebastian Walther, Direktor der Klinik für Psychiatrie, Psychosomatik und Psychotherapie, untersuchte mit Berner Kolleginnen und Kollegen, ob eine Kombination aus repetitiver transkranieller Magnetstimulation und sozialkognitiver Remediationstherapie (SCRT) helfen kann, diese Defizite zu verringern.
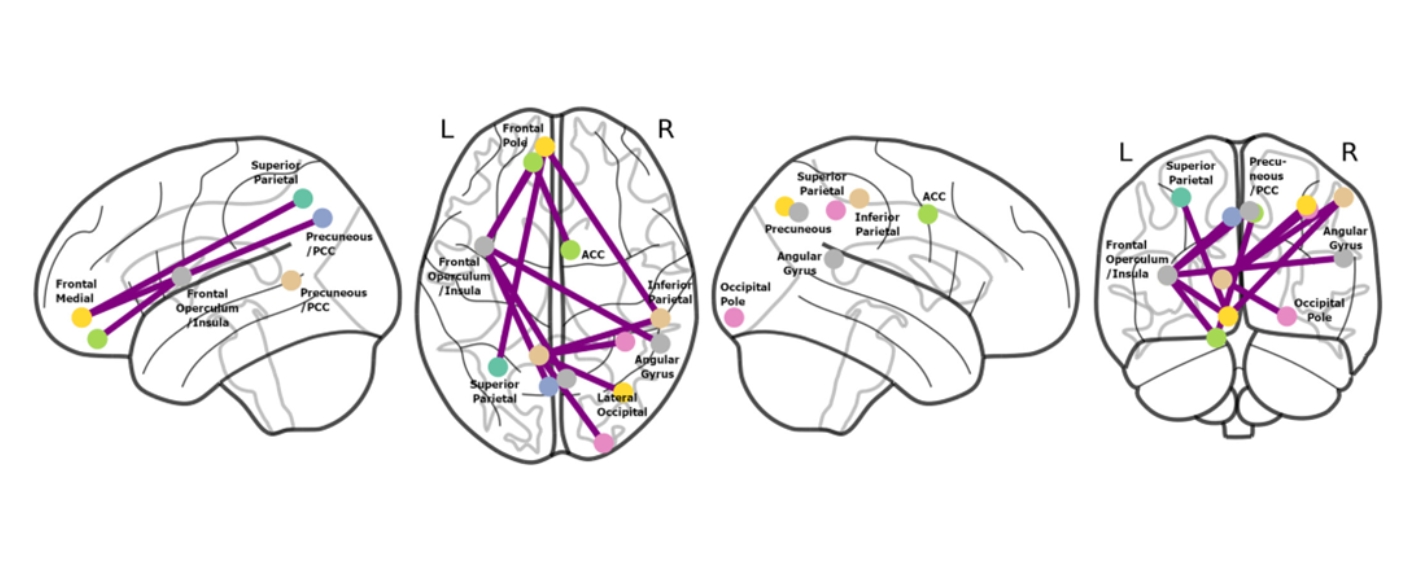
19 Teilnehmende erfuhren über einen Zeitraum von zwei Wochen zehn Sitzungen mit echter rTMS über den rechten unteren Parietallappen, der an der Steuerung von Gesten beteiligt ist. Diese Sitzungen wurden in Kombination mit 16 SCRT-Gruppensitzungen über einen Zeitraum von acht Wochen durchgeführt. 26 Teilnehmende erhielten eine Schein-rTMS in Kombination mit echter SCRT und 28 Personen eine Schein-SCRT.
Ergebnis: Ein soziales Miteinander allein ist bereits förderlich, wie die Kontrollgruppe mit Scheintherapien gezeigt hat. Besonders deutlich war der Effekt jedoch bei den Personen, die die Kombination aus echter rTMS und echter SCRT erhielten. In dieser Gruppe zeigten sich nicht nur Fortschritte bei bestimmten Gestenarten, insbesondere bei neu erlernten, bedeutungslosen Bewegungen, sondern auch eine spürbare Verbesserung der sozialen und alltagspraktischen Funktionsfähigkeit. Die positiven Effekte dieser sicheren und gut verträglichen Methode hielten auch Monate nach Ende der Behandlung an.
Details zur Studie liefert die Pressemeldung „Wieder in Verbindung treten“
Publikation:
Sebastian Walther, Lydia Maderthaner, Victoria Chapellier, Sofie von Känel, Daniel R. Müller, Stephan Bohlhalter, Mischa Baer & Anastasia Pavlidou. Gesture deficits in psychosis and the combination of group psychotherapy and transcranial magnetic stimulation: A randomized clinical trial. Molecular Psychiatry 30(12):5790-5799, https://www.nature.com/articles/s41380-025-03303-7, (2025)