Die Rolle von Inflammation, Autoimmunität und häufigen Virusinfektionen bei arrhythmogener Kardiomyopathie (A4)
Hintergrund
Arrhythmogene Kardiomyopathie (ACM) ist eine erbliche Herzmuskelerkrankung, die Zell-Zell-Kontakte und insbesondere kardiale Desmosomen betrifft. Es wurde gezeigt, dass Zellverbindungen infolge von Mutationen in desmosomalen Proteinen, aber auch als Reaktion auf kardiale oder systemische entzündliche Prozesse gestört sein können. Darüber hinaus weisen Betroffene mit einer ACM-Mutation häufig klinische Merkmale einer akuten Myokarditis auf, was darauf hindeutet, dass die genetische Veranlagung sowie deren Wechselwirkung mit Entzündungs- und Autoimmunreaktionen den Krankheitsprozess beeinflussen.
Unklare Rolle von Entzündung bei ACM
Patientinnen und Patienten mit ACM weisen neben den Symptomen einer Herzschwäche und Herzrhythmusstörungen manchmal auch Zeichen einer akuten oder chronischen kardiale Entzündung auf, die dann als "heiße Phase der Krankheit" gewertet wird. Allerdings ist die Rolle der Entzündung und des Immunsystems, sowie das Zusammenspiel mit den defekten Zell-Zellverbindungen und Signalwegen in der Pathogenese unklar.
Forschungsziel
Ziel ist es, die komplexen Wechselwirkungen zwischen gestörten kardialen Zell-Zell Verbindungen aufgrund
- mutierter desmosomaler Proteine
- kardialer und systemischer Entzündung sowie
- Autoimmunität
in der Pathogenese und im Verlauf der ACM zu untersuchen. Darüber hinaus werden wir analysieren, wie sich eine Infektion mit murinem CMV (MCMV) und ein positiver MCMV-Serostatus, also der Nachweis von bestimmten Antikörpern im Blut, auf die Entwicklung der Kardiomyopathie in genetisch prädisponierten Herzen auswirken.
Vorgehensweise
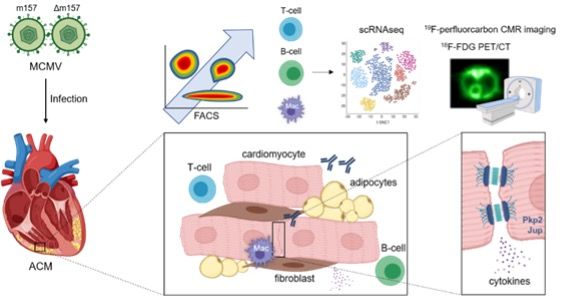
Wir untersuchen den Verlauf kardialer und systemischer Entzündungs- und Immunantworten während der Kardiomyopathieentwicklung. Dies geschieht unter anderem mithilfe der Durchflusszytometrie (FACS) und der Einzelzell-Sequenzierung (RNAseq) in knock-out Mausmodellen desmosomaler Proteine. Darüber hinaus bestimmen wir den Einfluss von entzündlichen Zytokinen auf Zell-Zell-Kontakte in iPSC-abgeleiteten Kardiomyozyten. Den Einfluss von viralen Infektionen als einen „second trigger“ erforschen wir unter Verwendung eines murinen CMV-Infektionsmodells.
Bedeutung und Ausblick
Vom Projekt A4 versprechen wir uns, dass unsere modellbasierten Erkenntnisse auf den Menschen mit ACM übertragbar sind und sich eine immunsuppressive sowie auch eine entzündungshemmende Therapie möglicherweise zukünftig als vorteilhaft erweist. Des weiteren glauben wir, dass Entzündungen und die adaptive Immunantwort auch bei anderen genetisch bedingten Kardiomyopathien eine Rolle spielen können und unsere Ansätze entsprechend richtungsweisend sein werden.
Anschrift
Medizinische Klinik und Poliklinik I, Universitätsklinikum Würzburg, Zentrum für Innere Medizin (ZIM), Oberdürrbacher Straße 6, Haus A3, 97080 Würzburg, Deutschland
Deutsches Zentrum für Herzinsuffizienz Würzburg | Comprehensive Heart Failure Center | Am Schwarzenberg 15 | Haus A15 | 97078 Würzburg


