Hintergrund
Neutrophile sind Zellen des angeborenen Immunsystems, die schnell in ein entzündetes Gewebe einwandern. Sie gelten als Hauptakteure bei einer akuten Entzündung. Neueste Studien weisen jedoch auch auf heilende Effekte hin. Ihre genaue Rolle und ob ihre Wirkung eher heilend oder schädlich ist, sowie der zeitliche Ablauf ihrer Aktivität bei der Entzündung nach einem Herzinfarkt sind noch weitgehend unbekannt. Um ein tieferes Verständnis für die Wirkung der Neutrophilen im entzündeten Gewebe zu erlangen und damit auch die Therapie zu verbessern, wollen wir ihre Migration über Positronen-Emissions-Tomographie (PET) sichtbar machen. Für dieses nicht-invasive Bildgebungsverfahren verwenden wir einen speziell entwickelten Radiotracer mit Fluor-18 als Radionuklid. Fluor-18 hat den Vorteil einer vergleichsweise langen Halbwertzeit von 110 Minuten, was eine Anwendung in der Klinik ermöglicht.
Forschungsziel
Wir wollen ein nicht-invasives, diagnostisches, molekulares Werkzeug entwickeln, das uns erlaubt, die Bewegung und Aktivität von Neutrophilen bei Entzündungsprozessen, wie etwa nach einem MI, zu beobachten. Dabei sollen neben der Lokalisierung auch die Intensität der Migration an verschiedenen Schnittstellen und Phasen der Entzündung messbar werden. Dazu planen wir die Synthese sowohl nichtradioaktiver „kalter“ als auch radioaktiv markierter „heißer“ Fluorderivate von bereits bekannten Liganden, die spezifisch an Neutrophile binden. Diese Liganden sollen in vitro sowie in vivo evaluiert werden.
Vorgehensweise
Zur Entwicklung eines solchen Tracers nutzen wir zunächst literaturbekannte „kalte“ Liganden, die spezifisch an Neutrophile binden. In deren Leitstruktur fügen wir dann Fluor-Atome an verschiedenen Stellen des Moleküls ein, um eine Serie von synthetisierten Molekülen zu erhalten. Diese Moleküle werden dann in einem Radioligand-Bindungsassay auf ihre Bindungsaffinität und in einem NanoBRET-Assay auf ihre Selektivität getestet. Der Ligand mit den besten Ergebnissen wird für die radioaktive Markierung ausgewählt. Nach erfolgreicher Markierung wird die „heiße“ Verbindung auf ihr Bindungsverhalten an Neutrophilen von Tier und Mensch getestet. In anschließenden Tierversuchen wird die Verteilung und Eliminierung des Tracers verfolgt und etwaige Verbesserungen noch auf molekularer Ebene vorgenommen.
Bedeutung und Ausblick
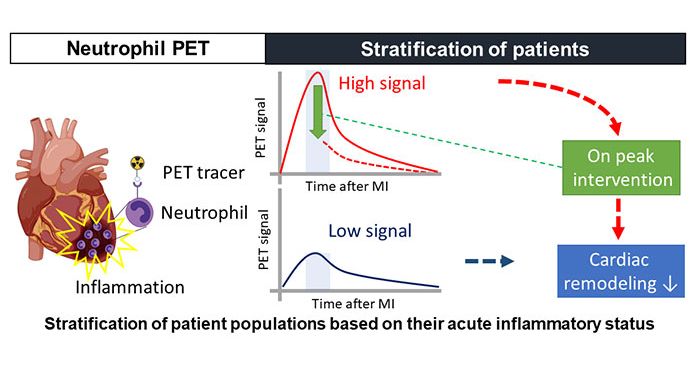
Ein geeigneter Radiotracer würde unser Verständnis von der Funktion der Neutrophilen während einer akuten Herzentzündung nach einem MI vertiefen. Das gewonnene Wissen kann anschließend zur Optimierung von Behandlungsstrategien genutzt werden.
Anschrift
Medizinische Klinik und Poliklinik I, Universitätsklinikum Würzburg, Zentrum für Innere Medizin (ZIM), Oberdürrbacher Straße 6, Haus A3, 97080 Würzburg, Deutschland
Deutsches Zentrum für Herzinsuffizienz Würzburg | Comprehensive Heart Failure Center | Am Schwarzenberg 15 | Haus A15 | 97078 Würzburg



