Pathomechanismen der spinalen Muskelatrophie
Untersuchungen haben ergeben, dass zwischen 90 und 95 Prozent der Fälle durch eine homozygote Mutation im SMN1-Gen auf dem humanen Chromosom 5 verursacht sind. Diese Region ist beim Menschen doppelt angelegt. Ein zweites SMN-Gen (SMN2) auf demselben Chromosom kann aufgrund eines Nukleotidaustausches im Exon-7 das Fehlen von SMN1 jedoch nicht vollständig kompensieren. Dies liegt darin begründet, dass nur ein geringer Teil der vom SMN2-Gen gebildeten Transkripte für ein voll funktionsfähiges SMN-Protein kodieren.
Mausmodell zeigt Auswirkungen der Erkrankung
Unsere Arbeitsgruppe hat erstmals ein Mausmodell für die SMA entwickelt und damit zeigen können, dass die Krankheit primär nicht das Überleben der Motoneuronen beeinträchtigt. Vielmehr wirkt sich die Erkrankung auf das Auswachsen und vor allem auf die funktionelle Aufrechterhaltung von axonalen Nervenzellfortsätzen und neuromuskulären Endplatten sowie auf die spezifischen Synapsen zwischen motorischen Nervenzellen und Skelettmuskelfasern aus.
Neue Zellkultursysteme
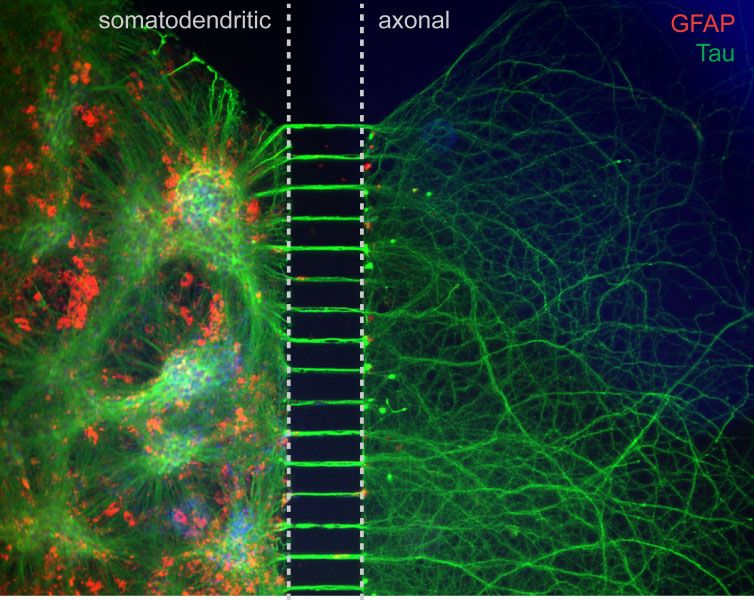
Die Arbeitsgruppe hat basierend auf diesen Ergebnissen neue Zellkultursysteme entwickelt, mit denen diese axonalen und präsynaptischen Defekte untersucht werden können. So fanden wir massive Veränderungen beim Transport der RNA aus dem Zellkörper in das axonale Kompartiment. Insbesondere Transkripte, die für Zytoskelettproteine wie Aktin-Isoformen sowie Komponenten des präsynaptischen Apparats für die Vesikelfreisetzung kodieren, sind betroffen und werden nicht in das axonale Kompartiment transportiert. Dies hat Auswirkungen auf die Kapazität von Motoneuronen, axonale Verzweigungen auszubilden sowie auf die Ausschüttung von Neurotransmittern für die Übertragung von Bewegungsimpulsen auf die Skelettmuskeln. Aktuell untersuchen wir Veränderungen im Transport spezifischer mRNAs der Komponenten präsynaptischer aktiver Zonen, wie sich diese Veränderungen auf die Synapsen auswirken und wie neue Methoden gefunden werden können, diese Defekte bei dieser Erkrankung zu kompensieren.
Ausgewählte Publikationen zu Pathomechanismen der spinalen Muskelatrophie
Briese M, Saal-Bauernschubert L, Changhe J, Moradi M, Ghanawi H, Uhl M, Appenzeller S, Backofen R, Sendtner M (2018)
hnRNP R and its main interactor, the noncoding RNA 7SK, coregulate the axonal transcriptome of motoneurons.
PNAS 115(12):E2859-E2868. doi: 10.1073/pnas.
Jablonka S, Sendtner M (2017)
Developmental regulation of SMN expression: pathophysiological implications and perspectives for therapy development in spinal muscular atrophy.
Gene Ther 24, 506-513.
Rossoll W, Jablonka S, Andreassi C, Kröning A-K, Karle K, Monani UR, Sendtner M (2003)
Smn, the spinal muscular atrophy-determining gene product, modulates axon growth and localization of ß-actin mRNA in growth cones of motoneurons.
J. Cell Biol 163, 801-812.
Saal L, Briese M, Kneitz S, Glinka M, Sendtner M (2014)
Subcellular transcriptome alterations in a cell culture model of spinal muscular atrophy point to widespread defects in axonal growth and presynaptic differentiation.
RNA 20, 1789-1802.
Schrank B, Götz R, Gunnerson JM, Ure JM, Toyka KV, Smith AG, Sendtner M (1997)
Inactivation of the survival motor neuron gene, a candidate gene for human spinal muscular atrophy, leads to massive cell death in early mouse embryos.
PNAS 94, 9920-9925.
Sendtner M (2010)
Therapy development in spinal muscular atrophy.
Nat. Neurosci. 13, 795-799.