RNA-Metabolismus in Nervenzellen
Subzelluläre RNA-Verteilung und lokale Proteinsynthese in Nervenzellen
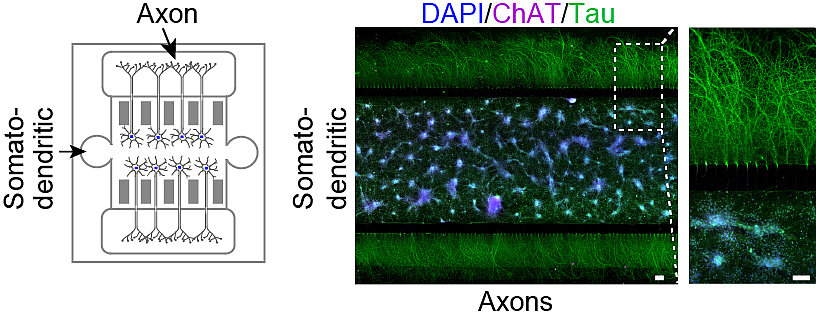
Nervenzellen sind hochpolar aufgebaut. Während Dendriten synaptischen Input von anderen Nervenzellen erhalten, leiten Axone die elektrischen Impulse weg vom Zellkörper über teils große Distanzen zu den verschalteten Zielzellen. Bei Motoneuronen kann ihre Länge das über Zehntausendfache des Durchmessers eines Zellkörpers erreichen. Diese axonalen Fortsätze sind weit verzweigt. In all diesen Bereichen können lokal Proteine an Ribosomen neu synthetisiert werden, die für die spezifischen Funktionen in diesen Regionen relevant sind. Die dafür notwendigen mRNAs werden vom Zellkörper in die Axone mit Hilfe von RNA-bindenden Proteinen transportiert.
Gestörter RNA-Transport als Mechanismus neurodegenerativer Erkrankungen
Unsere Arbeitsgruppe beschäftigt sich mit Mechanismen der subzellulären Verteilung von RNA und der Kontrolle der RNA-Translation in Axonen. RNA-Bindungsproteine wie hnRNP R und TDP-43 spielen bei der Prozessierung von RNA im Zellkern und dem RNA-Transport in Axonen eine wichtige Rolle. Eine Fehlfunktion dieser Prozesse ist Teil des Pathomechanismus von Motoneuronerkrankungen wie der Spinalen Muskelatrophie (SMA) oder der Amyotrophen Lateralsklerose (ALS). In unseren Forschungsprojekten haben wir die Verteilungsstörungen von mRNA-Molekülen in Motoneuronen untersucht, welche nach Beeinträchtigung von SMN, hnRNP R und TDP-43 auftreten. Auch Veränderungen in der Translationskontrolle für die lokale Proteinsynthese in Axonen wurden beobachtet. Diese Veränderungen führen dazu, dass Nervenimpulse nicht auf den Muskel übertragen werden können. Zu den wichtigen Zielen unserer Forschung zählt es, diese beeinträchtigte Funktion in axonalen Nervenzellfortsätzen zu verbessern oder wiederherzustellen.
Ausgewählte Publikationen zu RNA-Metabolismus
Zare A, Salehi S, Bader JM, Wiessler AL, Prokesch M, Albrecht V, Villmann C, Mann M, Briese M and Sendtner M (2025)
Axonal tau reduction ameliorates tau and amyloid pathology in a mouse model of Alzheimer's disease.
Transl Neurodegener 14: 39
Zare A, Salehi S, Bader J, Schneider C, Fischer U, Veh A, Arampatzi P, Mann M, Briese M and Sendtner M (2024)
hnRNP R promotes O-GlcNAcylation of eIF4G and facilitates axonal protein synthesis.
Nat Commun 15: 7430
Ji C, Deng C, Antor K, Bischler T, Schneider C, Fischer U, Sendtner M and Briese M (2022)
hnRNP R negatively regulates transcription by modulating the association of P-TEFb with 7SK and BRD4.
EMBO Rep 23: e55432
Ji C, Bader J, Ramanathan P, Hennlein L, Meissner F, Jablonka S, Mann M, Fischer U, Sendtner M and Briese M (2021)
Interaction of 7SK with the Smn complex modulates snRNP production.
Nat Commun 12: 1278
Briese M, Saal-Bauernschubert L, Luningschror P, Moradi M, Dombert B, Surrey V, Appenzeller S, Deng C, Jablonka S and Sendtner M (2020)
Loss of Tdp-43 disrupts the axonal transcriptome of motoneurons accompanied by impaired axonal translation and mitochondria function.
Acta Neuropathol Commun 8: 116