Würzburg. Alzheimer ist die häufigste Ursache von Demenz und zählt zu den größten Gesundheitsherausforderungen unserer Zeit. Bei dieser neurodegenerativen Erkrankung sterben Nervenzellen im Gehirn fortschreitend ab. Bislang konzentrierte sich die Alzheimer-Forschung vorwiegend auf die Amyloid-Plaques, die ein typisches Kennzeichen der Erkrankung sind. Die Wirksamkeit von Medikamenten, welche die Plaques reduzieren, ist jedoch umstritten. Daher fokussieren sich immer mehr Forscherinnen und Forscher auf das Tau-Protein, das nicht nur bei Alzheimer, sondern auch bei anderen neurodegenerativen Erkrankungen wie der Frontotemporalen Demenz (FTD) und der amyotrophen Lateralsklerose (ALS) verändert ist.
Hier ist das Institut für Klinische Neurobiologie des Universitätsklinikums Würzburg (UKW) nun einen wichtigen Schritt in der Forschung weitergekommen. Prof. Dr. Michael Sendtner, Privatdozent Dr. Michael Briese, Dr. Abdolhossein Zare und Dr. Saeede Salehi haben einen Schlüsselmechanismus zur Verhinderung schädlicher Tau-Ablagerungen im Gehirn entdeckt (bioRxiv - Preprint).
Mit 500.000 Euro dotierter „m4 Award” für Forschungsprojekte mit Ausgründungspotential
Dass eine Weiterentwicklung dieses Forschungsansatzes beträchtliches Potential für die Behandlung von Alzheimer hat, sieht auch das Bayerische Staatsministerium für Wirtschaft, Landesentwicklung und Energie. Staatssekretär Tobias Gotthardt und Prof. Dr. Ralf Huss, Geschäftsführer der BioM Biotech Cluster Development GmbH, überreichten am 2. Juli im Rahmen der Konferenz „BayOConnect” in München den mit 500.000 Euro dotierten „m4 Award” an die Arbeitsgruppe von Michael Briese und Michael Sendtner.
Der Preis richtet sich an akademische Forschungsprojekte mit Ausgründungspotenzial im Bereich der Biomedizin und wird alle zwei Jahre an fünf Teams vergeben. Mit der Förderung soll die Fähigkeit zu einer Anschlussfinanzierung erreicht werden. Alle ausgezeichneten Projekte erhalten zudem eine intensive Projektbegleitung auf dem Weg zur Unternehmensgründung.
Tau-Proteine stabilisieren das Zytoskelett, akkumulieren jedoch bei Alzheimer in den Axonen und führen so zum Absterben der Nervenzellen
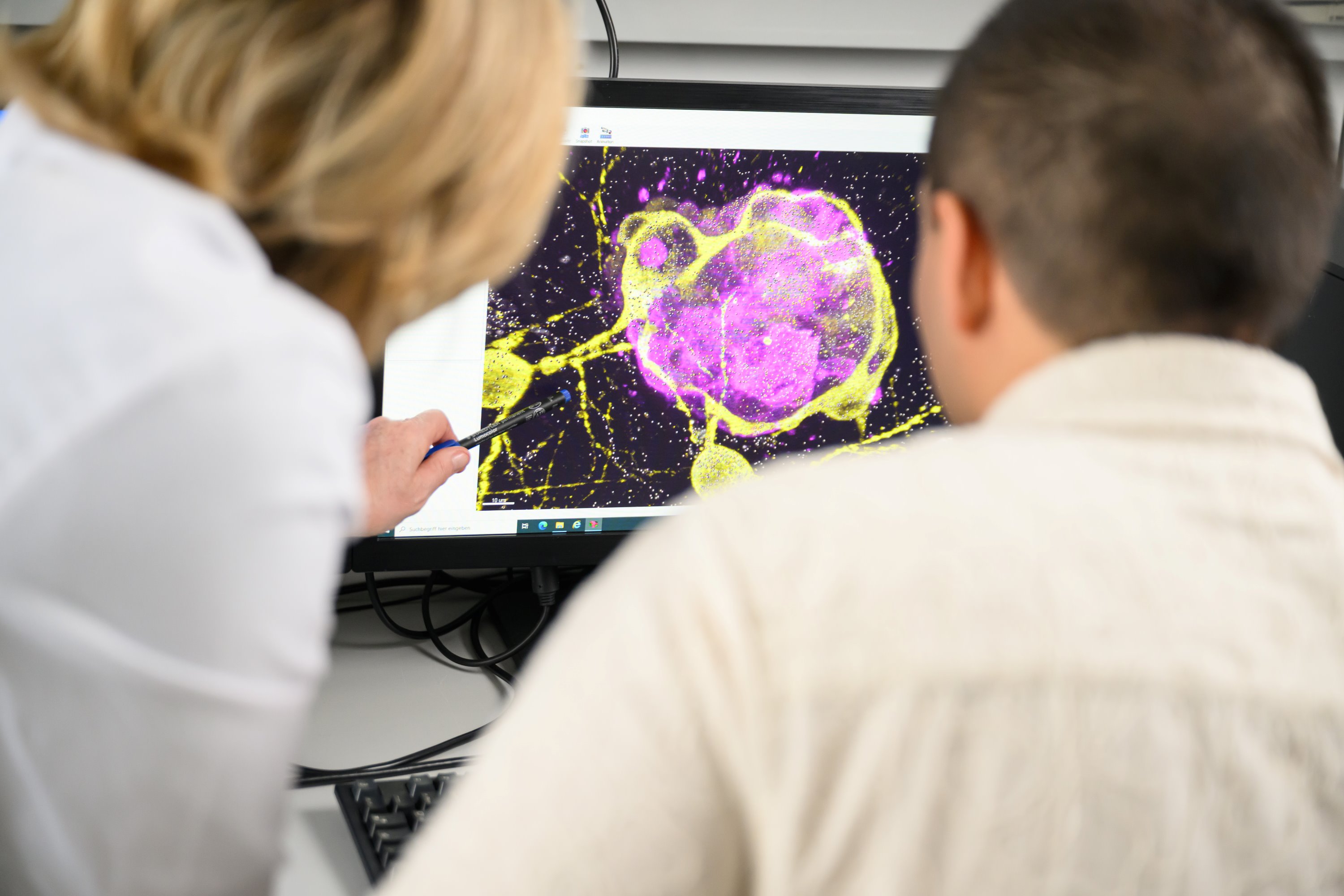
Doch was sind Tau-Proteine eigentlich? Die Preisträger klären auf: „Tau-Proteine stabilisieren normalerweise die Struktur von Nervenzellen, das sogenannte Zytoskelett. Bei der Alzheimer-Krankheit aggregiert das Tau-Protein jedoch in den langen Fortsätzen, den Axonen, wodurch der intrazelluläre Transport und somit die Zellfunktion gestört werden. Die Nervenzellen sterben nach und nach ab, was sich bei den Betroffenen durch Gedächtnisprobleme, Orientierungslosigkeit und später durch starke kognitive Beeinträchtigungen bemerkbar macht“, erläutert Michael Briese. Der Naturwissenschaftler bringt seine Expertise in der RNA-Forschung seit 2012 in die Projekte zu neurodegenerativen Erkrankungen am UKW ein. Er studierte in Großbritannien, promovierte bei David Sattelle an der University of Oxford (MRC Functional Genetics Unit) und arbeitete anschließend als Postdoc bei Jernej Ule am Medical Research Council (MRC) Laboratory of Molecular Biology in Cambridge.
Warum also Tau nicht komplett blockieren? „Weil es in den Dendriten benötigt wird, zumindest stärker als in den Axonen“, erklärt Michael Sendtner. Der Humanmediziner leitete von 1994 bis 1999 die Klinische Forschergruppe „Neurobiologie“ am UKW, war von 2000 bis 2012 Sprecher des Sonderforschungsbereichs 581 „Molekulare Modelle für Erkrankungen des Nervensystems“ und ist seit der Jahrtausendwende Direktor des Instituts für Klinische Neurobiologie. Im Gegensatz zu den Axonen, welche die Informationen vom Zellkörper weg zu anderen Nervenzellen oder Muskeln leiten, empfangen die kürzeren, stark verästelten und baumartig aufgebauten Dendriten die Informationen von anderen Nervenzellen und leiten sie zum Zellkörper weiter. „Würde man Tau auch in den Dendriten reduzieren, ginge es dem Behandelten genauso schlecht wie bei Alzheimer: Die Person kann nicht mehr klar denken und sich nicht mehr orientieren“, schildert Sendtner.
hnRNP R hilft dabei, die Tau-mRNA in das Axon der Nervenzelle zu transportieren
Man muss also verhindern, dass die Tau-mRNA, also der Bauplan für das Tau-Protein, aus dem Zellkern zum Axon kommt und gewährleisten, dass der Transport zum Dendrit ungehindert läuft. Michael Sendtner zieht zur Veranschaulichung der Transportblockade zum Axon das Beispiel einer Buslinie heran. Die eine Linie geht vom Zellkern zum Dendrit, die andere Buslinie zum Axon. Während Tau zum Dendrit freie Fahrt hat, wird dem Protein der Einstieg in den Bus zum Axon verwehrt.
Die Forscher schauten sich den Mechanismus genauer an. Eine Zufallsbeobachtung von Michael Briese führte schließlich zur bahnbrechenden Erkenntnis, dass das Protein hnRNP R der zentrale Transporter, also die Buslinie für die Tau-Baupläne zu den Axonen ist.
hnRNP R gehört zur Familie der heterogenen nukleären Ribonukleoproteine (hnRNP), die an RNA binden und eine wichtige Rolle bei der Verarbeitung der Erbinformationen im Zellkern spielen. „Wir haben beobachtet, dass sich hnRNP R an einen bestimmten Abschnitt der Tau-mRNA, den sogenannten 3'-UTR, anhängt. Weitere Untersuchungen an kultivierten Neuronen, in denen dieses Protein fehlt, zeigten, dass die Menge des Tau-Proteins spezifisch in den Axonen reduziert ist“, berichtet Briese.
Antisense-Oligonukleotide blockieren den Transportprozess und verhindern Bildung von Tau-Aggregaten im Axon, wodurch das Fortschreiten der Erkrankung gestoppt wird
Aus Neugier haben die Forscher sogenannte Antisense-Oligonukleotide (ASOs) entworfen, mit dem das Tau-Protein zielgenau in den Axonen reduziert werden kann. Bei ASOs handelt es sich um kurze (oligo), künstlich hergestellte Stränge aus DNA- oder RNA-Bausteinen (Nukleotide), die entgegengesetzt zur Leserichtung (antisense) der natürlichen mRNA sind. Sie binden sich komplementär an die mRNA, um diese zu blockieren.
Und siehe da: In den Zellkulturen hatten die ASOs einen „umwerfenden Effekt“, so Sendtner. Sie verhinderten die Bindung der Tau-mRNA an hnRNP R, sodass weniger Tau-mRNA in die Axone gelangt. Mit finanzieller Unterstützung der Stiftung VERUM testeten sie die ASOs in Mausmodellen. Auch hier waren die Effekte umwerfend. „Unser Wirkstoff konnte das Fortschreiten der Alzheimer-Erkrankung stoppen“, freut sich Michael Briese über diese Entdeckung. Sie stellt einen Meilenstein in der Karriere des Grundlagenwissenschaftlers dar.
Potential für einen klinischen Wirkstoff
Wenn ein ASO, das ursprünglich nur als Proof of Principle gedacht war, derart massive Effekte hatte, wie sehen diese dann nach einer Optimierung zum echten Medikamentenkandidaten in weiteren Mausmodellen und später bei Patientinnen und Patienten aus? Besteht vielleicht sogar die Chance, dass sich die eine oder andere Funktion verbessert, wenn die Krankheit nicht mehr fortschreitet und regenerative Prozesse angestoßen werden?
Die Forscher wandten sich an das Servicezentrum Forschung und Technologietransfer (SFT) der Julius-Maximilians-Universität Würzburg. Dieses half ihnen nicht nur bei der Patentanmeldung, sondern legte ihnen auch eine Bewerbung beim Vorgründungswettbewerb „m4 Award” nahe. Sendtner: „Für die optimale und hochprofessionelle Betreuung und Begleitung durch das SFT, insbesondere durch Dr. Iris Zwirner-Baier, Leiterin des Servicezentrums InterNationalTransfer, Erfinderberaterin und Patentmanagerin, sowie durch den Innovations-Scout Thorsten Zacher, möchten wir uns ganz herzlich bedanken. Ohne sie wären wir nicht da, wo wir jetzt sind.“ Und zwar im Forschungsprojekt mit dem Namen „blockALZ/MAPT-ASO – Blockade der axonalen Tau-Synthese als neuer Therapieansatz für die Behandlung der Alzheimer-Erkrankung“.
Der neu entwickelte Wirkstoff mit Potential zur Medikamentenentwicklung soll zunächst in Zellkulturen und später in einem Mausmodell getestet werden. Das unmittelbare Ziel der Ausgründung wäre das präklinische Testen und die Weiterentwicklung der Wirkstoffkandidaten bis hin zur klinischen Studie. „Wenn sich ähnlich gute Effekte zeigen, dann ist die Wahrscheinlichkeit sehr hoch, dass das Medikament auch beim Menschen anschlägt“, sagt Michael Sendtner. „Unser Therapieansatz ist nicht nur für die Alzheimer-Erkrankung, sondern auch für andere Tauopathien wie die frontotemporale Demenz relevant.“
Bevor die Forscher jedoch auf die Suche nach Investoren gehen, um das Medikament bis zur Marktreife weiterzuentwickeln, suchen sie noch eine Postdoktorandin oder einen Postdoktoranden mit Erfahrung im Bereich Stammzellen für die Kultivierung von humanen Neuronen. Bewerbungen gern an Michael Briese (Briese_M@ukw.de) oder Michael Sendtner (Sendtner_M@ukw.de).