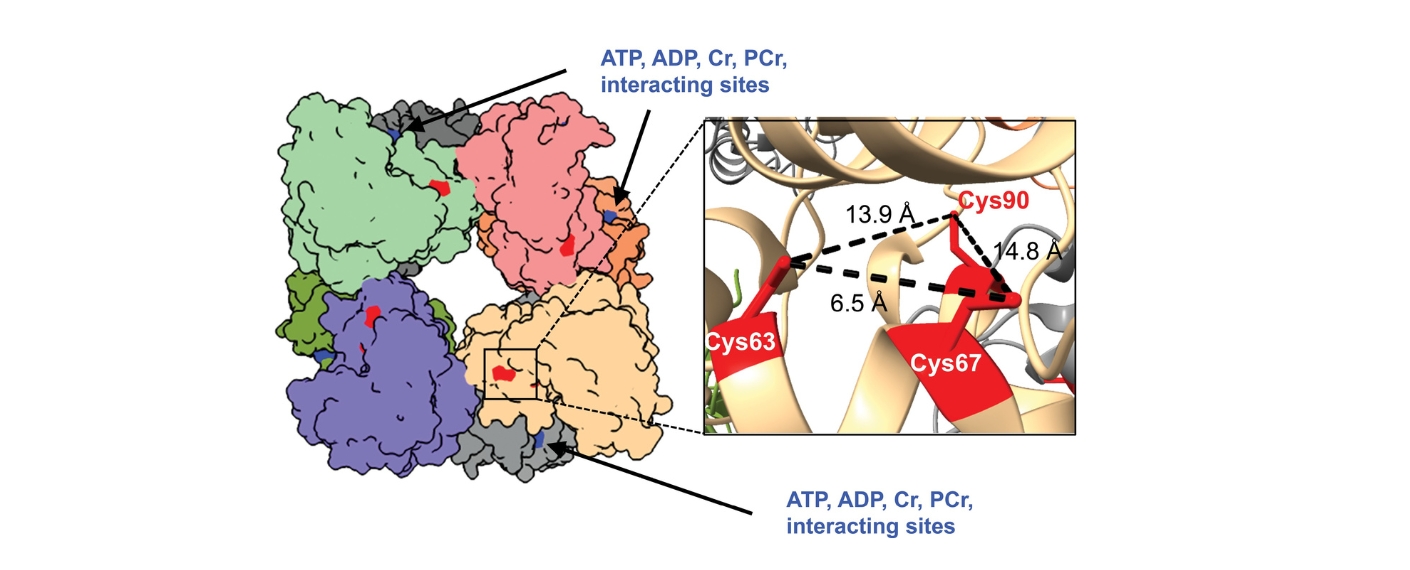
Die Forschenden rund um Anton Xu, Erstautor der Studie, und Vasco Sequeira, Letztautor, zeigen, dass die krankhaft erhöhte Kontraktionskraft des Herzmuskels zu oxidativem Stress in den Mitochondrien führt. Dabei wird das Enzym Kreatinkinase – zentral für den schnellen Energietransport im Herzen – an entscheidenden Stellen ausgeschaltet. Die Folge: Das energetische Gleichgewicht des Herzens gerät aus dem Takt, was das Risiko für gefährliche Herzrhythmusstörungen erhöht.
Besonders vielversprechend ist ein therapeutischer Ansatz mit sogenannten Myosinhemmern. Diese Medikamente reduzieren die übermäßige Muskelkontraktion, senken den oxidativen Stress, schützen die Kreatinkinase-Funktion und konnten in Modellen sowie in Patientenproben Herzrhythmusstörungen verringern. Künftige Arbeiten konzentrieren sich auf die hypertrophe obstruktive Kardiomyopathie (HOCM) und darauf, messbare Marker zu entwickeln, mit denen sich Patientinnen und Patienten identifizieren lassen, die besonders von dieser entlastenden Therapie profitieren könnten.
Details liefert die ausführliche Pressemeldung zur Publikation.
Publikation
Anton Xu, David Weissman, Katharina J. Ermer, Edoardo Bertero, Jan M. Federspiel, Felix Stadler, Elisa Grünler, Melina Tangos, Sevasti Zervou, Mark T. Waddingham, James T. Pearson, Jan-Christian Reil, Smita Scholtz, Jan Dudek, Michael Kohlhaas, Alexander G. Nickel, Lucie Carrier, Thomas Eschenhagen, Michelle Michels, Cris Dos Remedios, Sean Lal, Leticia Prates Roma, Nazha Hamdani, Diederik Kuster, Inês Falcão-Pires, Christopher N. Johnson, Craig A. Lygate, Jolanda van der Velden, Christoph Maack, Vasco Sequeira. Hypercontractility and Oxidative Stress Drive Creatine Kinase Dysfunction in Hypertrophic Cardiomyopathy, Circulation (American Heart Associationi), October 2025, https://doi.org/10.1161/CIRCULATIONAHA.125.074120