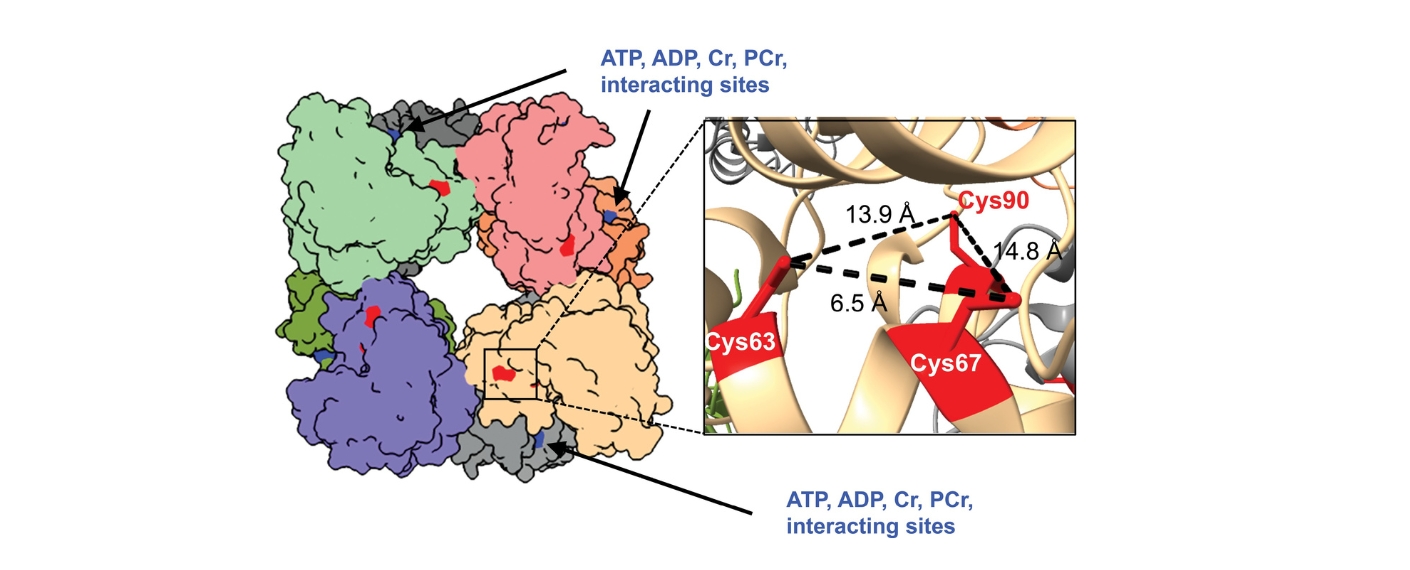
Das Forschungsteam rund um Prof. Dr. Niels Voigt (UMG) und Prof. Dr. Christoph Maack (DZHI) zeigt, dass eine gestörte Kommunikation zwischen zentralen Zellstrukturen des Herzmuskels eine Schlüsselrolle spielt. Konkret ist der Austausch von Kalzium zwischen dem sarkoplasmatischen Retikulum (ein feines Röhrchensystem innerhalb der Herzmuskelzelle, das Kalzium speichert und bei jedem Herzschlag freisetzt) und den Mitochondrien beeinträchtigt – mit weitreichenden Folgen für die Energieversorgung und elektrische Stabilität der Herzmuskelzellen.
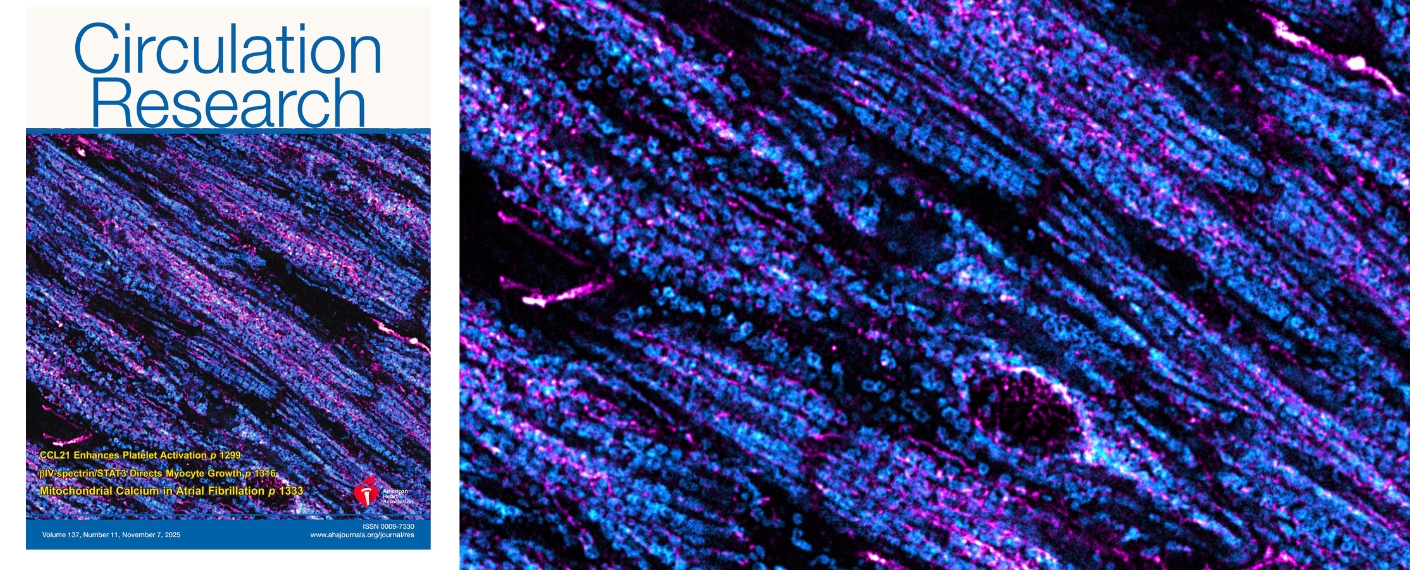
Bei Patientinnen und Patienten mit Vorhofflimmern nehmen die Mitochondrien weniger Kalzium auf, wodurch wichtige Energieträger schlechter regeneriert werden. Hochauflösende Bildgebung belegt zudem, dass die räumliche Nähe zwischen den „Kraftwerken der Zelle“ und dem Kalziumspeicher verloren geht. Das Herz gerät dadurch energetisch und elektrisch aus dem Gleichgewicht.
Ein überraschender Befund der Studie: Ein bereits zugelassenes cholesterinsenkendes Medikament konnte die Kalziumaufnahme der Mitochondrien teilweise wieder verbessern. Daten aus Patientengruppen deuten zudem darauf hin, dass Menschen unter dieser Therapie seltener an Vorhofflimmern erkranken. Die Ergebnisse, veröffentlicht in Circulation Research, eröffnen neue Perspektiven für gezielte Behandlungsansätze, die auf die Stabilisierung der zellulären Energie- und Kalziumhaushalte abzielen.
Weitere Informationen liefert die Pressemeldung zur Publikation.
Publikation
Julius Ryan D. Pronto, Fleur E. Mason, Eva A. Rog-Zielinska, Funsho E. Fakuade, Donata Bülow, Marcell Tóth, Khaled Machwart, Paulina Brandes, Felix Wiedmann, Michael Kohlhaas, Alexander Nickel, Matthias Wolf, Julian Mustroph, Kim-Chi Vu, Sören Brandenburg, Tri Q. Do, Peter Joshua Siedler, Katharina Ritzenhoff, Zongqian Xue, Xiaobo Zhou, Stefanie Kestel, Olga Dschun, Oksana Kyshynska, George Kensah, Robyn T. Rebbeck, Aschraf El-Essawi, Ahmad Fawad Jebran, Bernhard C. Danner, Hassina Baraki, Johann Schredelseker, Ivan Bogeski, Bianca J.J.M. Brundel, Stephan E. Lehnart, Constanze Bening, Ingo Kutschka, Felix Bremmer, Stefan M. Kallenberger, Silvio O. Rizzoli, Björn C. Knollmann, Stefan Neef, Katrin Streckfuss-Bömeke, Constanze Schmidt, Christoph Maack, and Niels Voigt. Impaired Atrial Mitochondrial Calcium Handling in Patients With Atrial Fibrillation. Circulation Research (2025). DOI: https://doi.org/10.1161/CIRCRESAHA.124.325658