Da bei Frühgeborenen nur sehr kleine Blutmengen entnommen werden können und die Kohorten sehr heterogen sind, fehlen belastbare Daten darüber, wie sich die verschiedenen Zellarten des adaptiven Immunsystems, insbesondere T- und B-Zellen, nach der Geburt entwickeln.
Diese Studie hat dieses Problem aufgegriffen, indem Immunzellen im Blut von Frühgeborenen untersucht wurden, die ohnehin im Rahmen der Routineversorgung auf der Neugeborenen-Intensivstation Blutabnahmen erhielten. Die Ergebnisse wurden anschließend mit verschiedenen Faktoren rund um die Geburt in Beziehung gesetzt.
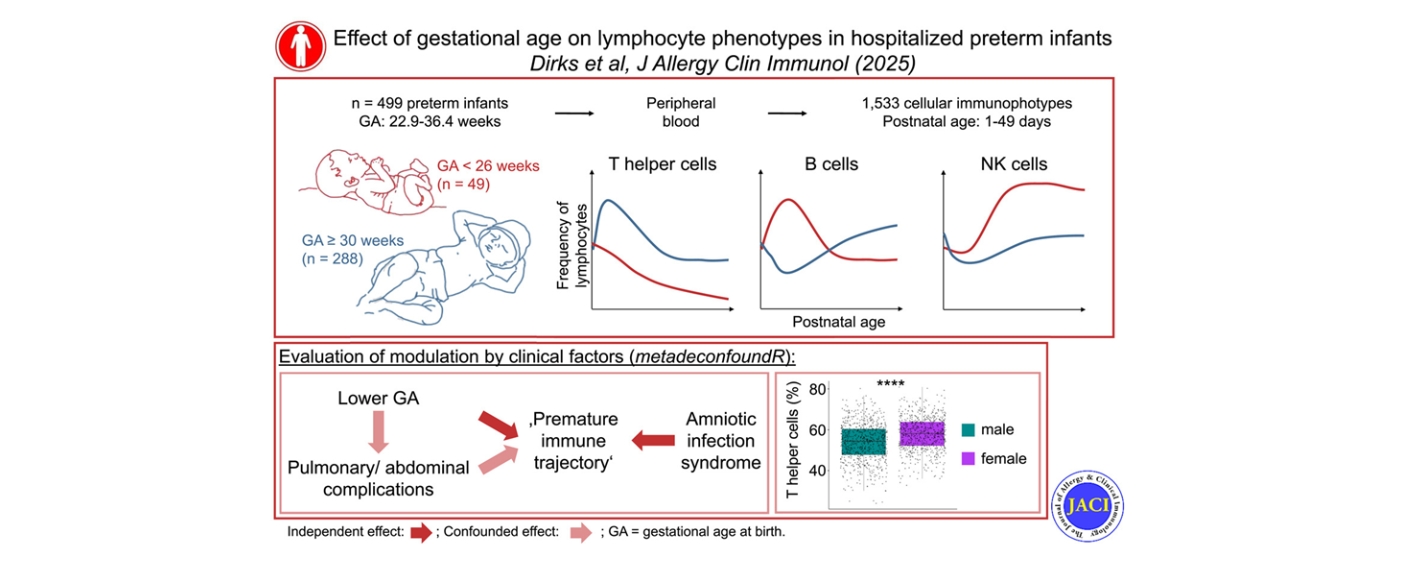
Insgesamt wurden über 1500 Blutuntersuchungen aus den ersten 50 Lebenstagen von 577 Frühgeborenen ausgewertet. Die Kinder wurden mit einem Schwangerschaftsalter (Gestationsalter) zwischen 22 und 36 Wochen und einem Geburtsgewicht zwischen 305 und 2820 Gramm an den Unikliniken Lübeck und Würzburg geboren. Die Auswertung zeigte klar: Der wichtigste Einflussfaktor für die frühe Entwicklung des Immunsystems ist, wie früh ein Kind geboren wird. Je unreifer ein Kind bei der Geburt ist, desto stärker und länger unterscheiden sich seine Immunzellen von denen reiferer Frühgeborener. Diese Unterschiede gleichen sich in den ersten Lebenswochen nicht aus.
Besonders unreif geborene Kinder zeigten dauerhaft niedrigere Anteile sogenannter CD4+ T-Helferzellen, die eine zentrale Rolle bei der Steuerung von Immunreaktionen spielen. Gleichzeitig fanden sich in den ersten Lebenswochen erhöhte Anteile von B-Zellen, gefolgt von einem späteren Anstieg natürlicher Killerzellen. Dieses charakteristische Muster deutet auf ein funktionell verändertes, aber nicht inaktives Immunsystem hin. In einer vertieften Analyse zeigte sich zudem, dass bei sehr früh geborenen Kindern weniger naive, neu gebildete T-Zellen vorhanden sind, während stärker aktivierte und regulierende T-Zelltypen häufiger auftreten. Dies spricht für eine veränderte Reifung und Neubildung von Immunzellen bereits früh nach der Geburt.
Neben dem Gestationsalter beeinflussten weitere Faktoren das Immunsystem. Eine Entzündung kurz vor Geburt, das sogenannte Amnioninfektionssyndrom, verstärkte die immunologischen Veränderungen zusätzlich. Auch typische Komplikationen der Frühgeburtlichkeit gingen mit ähnlichen Immunprofilen einher. Auffällig war außerdem ein Geschlechtsunterschied: Frühgeborene Mädchen wiesen durchgehend höhere Anteile an T-Helferzellen auf, was möglicherweise zu ihrem insgesamt besseren Überleben beiträgt.
Zusammenfassend zeigt die Studie, dass die Entwicklung des Immunsystems bei Frühgeborenen stark vom Zeitpunkt der Geburt geprägt wird und durch Entzündungen vor der Geburt sowie durch das Geschlecht weiter beeinflusst werden kann. Als bisher größter veröffentlichte Datensatz der postnatalen Entwicklung von adaptiven Abwehrzellen liefert die Studie wichtige Referenzwerte für die klinische Einordnung von Immunbefunden, die zum Beispiel bei auffälligen Befunden im seit 2019 bei allen Neugeborenen durchgeführten Screening auf angeborene schwere kombinierte Immundefekte erhoben werden. Darüber hinaus tragen die Ergebnisse zum besseren Verständnis der Ursachen der besonderen Infektionsanfälligkeit dieser vulnerablen Patientengruppe bei.
Publikation:
Johannes Dirks, Ingmar Fortmann, Janina Marißen, Julia Pagel, Lilith Reichert, Henry Kipke, Marie-Theres Dammann, Wolfgang Göpel, Till Birkner, Kilian Dahm, Sofia Kirke Forslund-Startceva, Dorothee Viemann, Jan Rupp, Henner Morbach, Christoph Härtel. Effect of gestational age on lymphocyte phenotypes in hospitalized preterm infants, Journal of Allergy and Clinical Immunology, 2025, ISSN 0091-6749, https://doi.org/10.1016/j.jaci.2025.09.030.