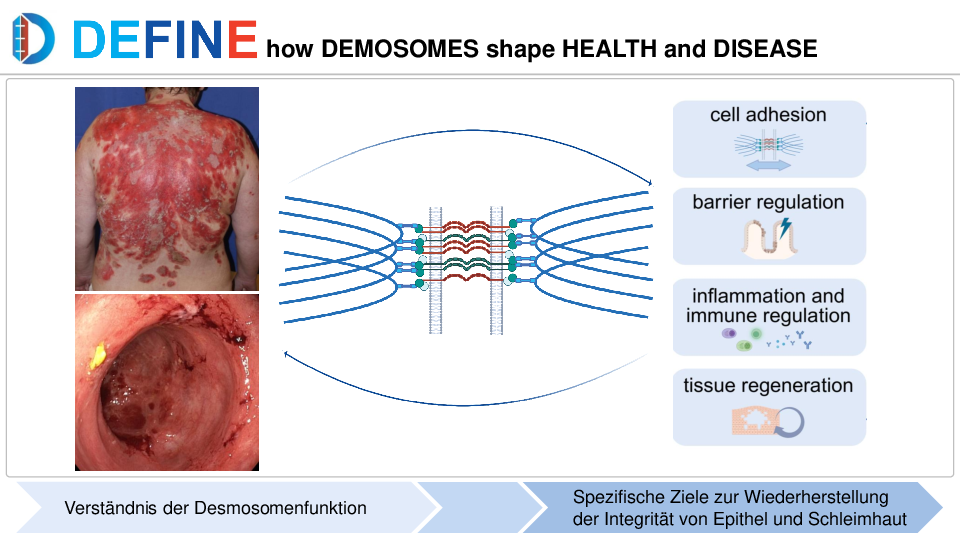
Die Universitätsmedizin Würzburg darf sich gemeinsam mit der Universität Marburg und der LMU München über die Bewilligung des neuen Sonderforschungsgereich Transregio „Desmosomal dysfunction in epithelial barriers” (DEFINE) freuen. Die Deutsche Forschungsgemeinschaft DFG fördert den SFB TRR von 2026 bis 2029 mit voraussichtlich rund 14 Millionen Euro. Im Mittelpunkt stehen Desmosomen. Diese Proteinstrukturen vernetzen Zellen an den Grenzflächen des Körpers miteinander und tragen so zur Bildung von Barrieren im Körper bei. Funktionierende Barrieren in der Haut und im Darm sind lebenswichtig, sodass bei deren Fehlfunktionen schwerwiegende Erkrankungen wie die lebensgefährliche Autoimmunkrankheit der Haut Pemphigus vulgaris, chronisch-entzündliche Darmerkrankungen sowie Entzündungen der Speiseröhre (eosinophile Ösophagitis) entstehen. Die Forschenden haben mit dem SFB nun die Möglichkeit, das noch sehr begrenzte Wissen über die Regulation von Epithelbarrieren bei Gesundheit und Krankheit deutlich zu erweitern und neuartige therapeutische Strategien gegen die drei genannten Krankheiten zu entwickeln.
Ein Interview mit dem Standortsprecher in Würzburg, Professor Nicolas Schlegel, Lehrstuhlinhaber für Experimentelle Viszeralchirurgie und Sektionsleiter Endokrine Chirurgie an der Klinik für Chirurgie I des Universitätsklinikums.
Herr Schlegel, herzlichen Glückwunsch zum neuen SFB/TRR DEFINE. Beteiligt sind die Universitätsstandorte Marburg, München und Würzburg. Wer hatte denn die Idee zu diesem Verbundprojekt?
Die Idee kam um die Weihnachtszeit 2021 in einem Steak-Restaurant in Würzburg, als ich mich mit Jens Waschke zu unserem regelmäßigen Austausch traf. Jens hatte in Würzburg den Lehrstuhl für Anatomie und Zellbiologie inne, bevor er 2011 den Ruf der LMU München auf den Lehrstuhl für vegetative Anatomie annahm. Wir arbeiten schon sehr lange zusammen und hatten ein Projekt im von der DFG geförderten Schwerpunktprogramm SPP 1782. Dabei hatten wir uns bereits eingehend damit beschäftigt, wie Zellen in Geweben über Desmosomen miteinander kommunizieren und auf Belastungen reagieren und wie Veränderungen dieser Desmosomen die Stabilität und Barrierefunktion des Gewebes beeinflussen. Wir überlegten, wie wir unsere Forschung nach dem Auslaufen des Programms fortsetzen und einen Schritt weiterkommen könnten.
Und da dachten Sie sich, wenn es jemals einen Sonderforschungsbereich zu diesem Thema geben kann, dann jetzt. Wie kam Michael Hertl, Direktor der Hautklinik des Universitätsklinikums Gießen und Marburg dazu?
Jens Waschke und Michael Hertl leiteten gemeinsam die DFG-Forschungsgruppe Pegasus, in dem sie das Krankheitsbild Pemphigus vulgaris untersuchten. Dabei handelt es sich um eine seltene, potenziell lebensbedrohliche Autoimmunerkrankung von Haut und Schleimhäuten. Bei ihrer Entstehung spielen Desmosomen in der Haut eine entscheidende Rolle. Diese werden nämlich fälschlicherweise von Antikörpern der eigenen Immunzellen angegriffen.
Sie konzentrieren sich jedoch auf die Desmosomen, die bei entzündlichen Darmerkrankungen eine Rolle spielen. Sie haben maßgeblich zur Entdeckung beigetragen. Wie passt das zusammen?
Wir fanden die Idee interessant, die Erkrankung der Haut, über die man bereits viel weiß, den Desmosomenveränderungen im Darm, über die noch nicht so viel bekannt ist, gegenüberzustellen. Was ist im Darm anders als in der Haut? Gibt es gemeinsame Nenner? Was sind gewebespezifische und was sind allgemeine Eigenschaften? Noch im Steakhaus haben wir einen Schmierzettel erstellt, Arbeitsgruppenleiter überlegt und die Idee an Michael Hertl herangetragen. Der war sofort Feuer und Flamme.
Wie ging es mit dem Projektantrag weiter – von der Idee bis zur Umsetzung?
Wir lernten uns kennen, erstellten ein Konzept und luden im Juli 2022 alle potenziellen Projektleiter zu einem zweitägigen Treffen ein. Im Herbst reichten wir die erste Skizze ein. Nach der Begutachtung fand im Juli 2023 das erste Beratungsgespräch statt, in dem wir positives Feedback zur wissenschaftlichen Fragestellung erhielten. Wir mussten jedoch noch einige strukturelle Aspekte nachschärfen, zum Beispiel die Nachwuchsförderung, sowie wissenschaftliche Details zur Qualitätssicherung. Im Herbst 2023 gaben wir die überarbeitete Skizze ab. Im Juli 2024 fand das zweite Beratungsgespräch statt, bei dem die Gutachter uns mit einem sehr positiven Feedback bedachten. Nachdem unser Projekt im November 2024 durch den Senat gegangen war, wurden wir zur Einreichung des Vollantrags aufgefordert. Das heißt, wir hatten bis Juni 2025 Zeit, einen 400 Seiten starken Projektantrag zu erstellen und einzureichen. Im September 2025 erfolgte in Marburg zunächst die Begutachtung des allgemeinen Konzepts, dann der Zentralprojekte und schließlich der Einzelprojekte. Das war mit großer Anspannung und extrem viel Vorbereitung verbunden. Aber wir sind sehr gut bewertet worden. Im November kam schließlich und zur großen Freude die offizielle Bewilligung durch die DFG.
Ein Alleinstellungsmerkmal ist, dass dieser SFB derzeit der einzige in Deutschland ist, der maßgeblich unter chirurgischer Federführung entstand.
Das Besondere ist, dass wir nicht nur ein solches grundlagenwissenschaftliches Projekt zu diesem speziellen Thema unter chirurgischer Federführung entwickelt haben, sondern dass auch sechs Projektleiter aus der Würzburger Chirurgie involviert sind. Sie sind alle in der Klinik aktiv und arbeiten als Clinician Scientists.
Die Interdisziplinarität des Projekts wurde besonders betont und gelobt. Es wurden viele unterschiedliche Fächer zusammengebracht. Welche Disziplinen sind denn konkret involviert?
Das ist es, was aus unserer Sicht den SFB ausmacht. Wir haben Expertinnen und Experten aus ganz unterschiedlichen Fächern zusammengebracht, die sonst nicht so eng miteinander arbeiten. Neben der Chirurgie und Dermatologie sind beispielsweise auch die Pädiatrie, Gastroenterologie und Kardiologie vertreten. Die klinische Expertise wird durch Zellbiologie und Immunologie ergänzt. Auch Biophysiker sind dabei, die uns dabei helfen, grundlegende Aspekte von Epithelzellen zu verstehen. Unser Ziel ist es, diese Riesenbrücke vom Einzelmolekül in die Klinik zu schlagen. Das ist unsere Perspektive für die nächsten zwölf Jahre.
Der SFB kann maximal zweimal um jeweils vier Jahre verlängert werden. Bei jeder Verlängerung soll die Projektleitung wechseln. Sind damit alle drei Standorte gleichberechtigt?
Ja, wir verstehen uns als Team und arbeiten auf Augenhöhe. Die Leitung haben wir nach Alter bestimmt. Michael ist der älteste von uns drei Sprechern und hat deshalb in der ersten Förderperiode den Lead. In der zweiten Phase, die hoffentlich gefördert wird, soll Jens Waschke als Zweitältester die Leitung übernehmen. Ich als Jüngster würde dann in der dritten Periode den Lead haben.
Kommen wir nun zum Würzburger Schwerpunkt, den chronischen Darmentzündungen. Welche klinischen Symptome haben die Betroffenen?
Die Patienten haben schwere Durchfälle, bis zu zehn am Tag, die teilweise blutig sein können. Sie leiden unter Bauchkrämpfen und Gewichtsabnahme, betroffene Kinder zudem unter Gedeihstörungen. Eine langjährige Entzündung kann sich zudem zu Darmkrebs entwickeln. Von der Krankheit sind etwa 10 bis 15 von 100.000 Personen betroffen, wobei chronische Darmentzündungen vor allem in der westlichen Welt stetig zunehmen. Man geht davon aus, dass das Epithel durch Umweltfaktoren und den westlichen Lebensstil, insbesondere das Ernährungsverhalten und die damit einhergehenden Veränderungen des Darmmikrobioms, beeinflusst wird.
Laien stellen sich vor, dass ein Viszeralchirurg den entzündeten Abschnitt des Darms entfernt. Im Projekt geht es jedoch nicht nur um die chirurgische Therapie. Worum geht es konkret?
Eine Störung der Darmepithelbarriere ist ein zentraler Grund dafür, dass Patienten überhaupt erst krank werden. Dies ist ein Problem, das wir bisher nicht therapeutisch adressieren können. Wir können zwar den entzündeten Darmabschnitt herausoperieren und Medikamente geben, die das Immunsystem unterdrücken. Diese Medikamente wirken jedoch nur bei 50 bis 60 Prozent der Betroffenen und haben darüber hinaus starke Nebenwirkungen. Wenn wir aber in der Lage sind, das Darmepithel über das Verständnis der Funktion von Desmosomen und allem, was damit zusammenhängt, zu stabilisieren und die Entzündung einzudämmen, könnten wir diese möglicherweise durch eine zusätzliche Therapie in den Griff bekommen.
Kurz zur Begriffserklärung. Was ist die Darmepithelbarriere?
Die Darmepithelbarriere ist eine Zellschicht, die die Innenseite des Darms auskleidet. Sie verhindert, dass die zahlreichen Bakterien, die normalerweise im Darm leben, in den Körper gelangen. Dieser Vorgang wird als Translokation bezeichnet. Verändert sich die Darmflora oder gewinnen krankheitserregende Keime überhand, kann es zu einer Störung des Darmepithels kommen. Dies kann wiederum dazu führen, dass solche Translokationen stattfinden und schwerwiegende Entzündungen im Darm ausgelöst werden. Die Dichtigkeit des Darmepithels ist also von entscheidender Bedeutung. Sie wird durch zwei Komponenten gewährleistet: die Epithelzelle selbst und die Zell-Zell-Kontakte. Und daran arbeiten wir.
Welche Rolle spielen hier die Desmosomen?
Die Desmosomen gehören zu den Verbindungen, mit denen sich die Epithelzellen gegenseitig festhalten und somit für eine gewisse Stabilität sorgen. Daneben gibt es noch die Tight Junctions, die vor allem dafür zuständig sind, den schmalen Raum zwischen den Zellen abzudichten, sodass nichts hindurchgelangen kann.
Den Desmosomen schrieb man viele Jahre lang eine Art Kleberfunktion zu. In den vergangenen Jahren hat sich jedoch gezeigt, dass sie neben dieser Funktion viele Prozesse im Epithel regulieren und die Regeneration des Darmepithels sowie die Differenzierung von Zellen beeinflussen. Sie ermöglichen überhaupt erst, dass Tight Junctions das Darmepithel abdichten.
Die Desmosomen scheinen also eine Art Schlüsselfunktion für die Aufrechterhaltung der Darmbarriere zu haben.
Richtig. Wenn wir diese Schlüsselfunktion genau verstehen, können wir hoffentlich spezifische Therapien entwickeln, die die Darmepithelbarriere stabilisieren. Bislang wissen wir, dass dies über Transmembranproteine, die sogenannten Desmogleine, calciumabhängig im Zwischenzellraum geschieht. Diese Proteine greifen wie kleine Ärmchen zwischen den Zellmembranen ineinander und verbinden die Zellen. Innen in der Zelle sind diese Verbindungen an Plaque-Proteine gekoppelt. Diese leiten einerseits Signale weiter und koppeln andererseits die Verbindung an das innere Zellskelett, wodurch die Zelle besonders stabil wird und das Gewebe widerstandsfähig ist.
Bei Entzündungen sind diese Desmosomen wesentlich herunterreguliert. Wir wollen herausfinden, aus welchen Gründen sie verschwinden und welchen Krankheitswert es tatsächlich hat, wenn Desmosomen nicht mehr vorhanden sind. Unsere Ergebnisse können wir dann gegebenenfalls auch auf andere Erkrankungen übertragen, bei denen Desmosomen eine Rolle spielen.
Können Sie Beispiel nennen, wie und mit wem sie das herausfinden wollen?
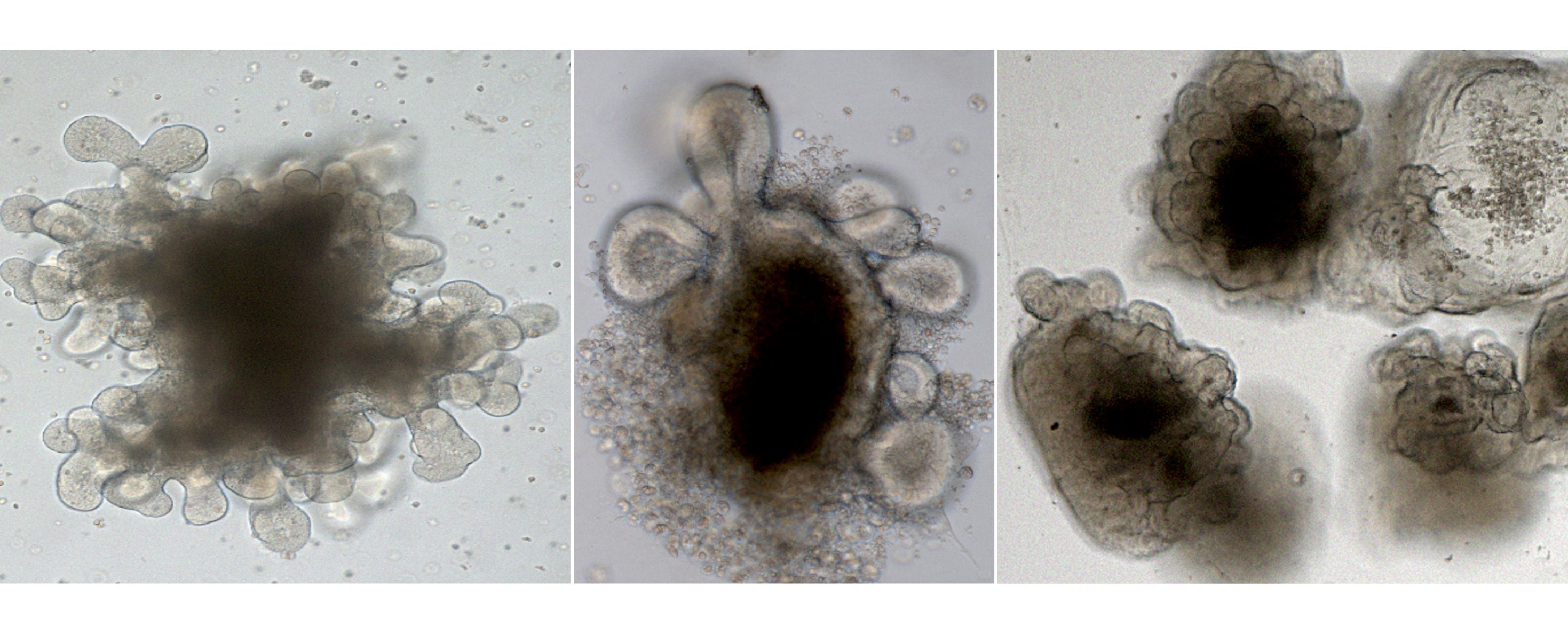
Unsere Projektleiter haben sich auf verschiedene Untereinheiten dieser Desmosomen fokussiert und untersuchen zellbiologische Aspekte mit verschiedenen Modellen - an Organoiden, Tiermodellen und Knock-out-Modellen. Mit Benjamin Misselwitz aus München haben wir beispielsweise einen weiteren Darmexperten an Bord. Er ist Professor für chronisch-entzündliche Darmerkrankungen in der Gastroenterologie und unter anderem in einem Zentralprojekt dafür zuständig, Proben aus Patientenmaterial für uns untersuchbar zu machen. Im Gegenzug bringt zum Beispiel Professor Goebeler, Direktor der Würzburger Hautklinik, seine dermatologische Expertise ein.
Was bedeutet der SFB speziell für Würzburg – abgesehen von den Fördergeldern?
Für mich geht es nicht nur um Gelder, sondern auch um Strukturen. Wir haben hier in Würzburg einen sehr starken immunologischen Schwerpunkt. Zur Immunologie gehört nicht nur das Immunsystem, sondern auch die Barrieren, die der Körper physiologisch aufrechterhalten muss. Diese müssen wir verstehen, adressieren und in den Kontext setzen. Warum entstehen entzündliche Erkrankungen? Wie beeinflussen sie Tumorerkrankungen, die ja auch hier am Standort intensiv untersucht werden? Unser SFB geht and dieser Stelle noch mehr in die Grundlagenwissenschaft und kann eine wichtige Lücke am Standort schließen.
Sie hatten bereits die Nachwuchsförderung angesprochen. Ein Teil des Zentralprojekts, das sich speziell mit diesem Thema beschäftigt, ist in Würzburg angesiedelt. Die Sprecherin ist Stefanie Hahner. Als langjährige Prodekanin der Medizinischen Fakultät kümmert sich die stellvertretende Leiterin der Endokrinologie um die Förderung des wissenschaftlichen Nachwuchses.
Die Nachwuchsförderung in Würzburg ist bereits sehr stark und wird durch den SFB sowie die sogenannte „Integrated Research Training Group“ (IRTG) weiter ausgebaut. Dieses Programm ist mir persönlich sehr wichtig. Denn hier bringen wir Mediziner und Naturwissenschaftler bereits auf der frühesten Karrierestufe zusammen. Eine frühe Verbindung der verschiedenen Sichtweisen – Klinik und Naturwissenschaften – kann sehr erfolgreich sein, wurde im Alltag jedoch lange vernachlässigt.
Die Grundlagenforscher haben oft tolle Tools, ihnen fehlt jedoch der direkte Link in die Klinik und umgekehrt. Das wollen wir mit einer frühen Verknüpfung untereinander ändern. Die IRTG ist aber auch an den anderen Standorten mit aktiven Leitern vertreten, so dass über alle 3 Standorte hinweg die gleichen Ideen gelebt werden.
Das Interview führte Kirstin Linkamp von der Wissenschaftskommunikation am UKW.